题目内容
【题目】现有一不纯的氧化铜样品16g,可能混有氧化铁、氧化镁、木炭粉、氯化钠中的一种或几种,加入200g稀硫酸恰好完全反应,没有固体剩余,生成3.6g水,则下列判断不正确的是( )
A. 原固体样品中肯定不含有木炭粉B. 原固体样品中混有的杂质可能有氯化钠
C. 所用的稀硫酸中溶质质量分数为9.8%D. 恰好完全反应后溶液中水的质量为184g
【答案】B
【解析】
氧化铜和稀硫酸反应生成硫酸铜和水,氧化铁和稀硫酸反应生成硫酸铁和水,氧化镁和稀硫酸反应生成硫酸镁和水,木炭和氯化钠不能反应,和稀硫酸也不能反应。
A、加入200g稀硫酸恰好完全反应,没有固体剩余,说明原固体样品中肯定不含炭粉,故A正确;
B、

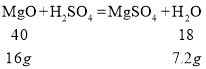
16g氧化铜和稀硫酸反应生成3.6g水,16g氧化铁和稀硫酸反应生成5.4g水,16g氧化镁和稀硫酸反应生成7.2g水,加入200g稀硫酸恰好完全反应,没有固体剩余,生成3.6g水,则可能含有氧化镁,也可能含有氧化铁,但一定含有氯化钠,故B不正确;
C、设硫酸的质量为x,生成的水中的氢元素完全来自于硫酸,则

![]()
x=19.6g
恰好完全反应后溶液中水的质量为![]()
所用硫酸的质量分数为 ![]() ,故C正确;
,故C正确;
D、恰好完全反应后溶液中水的质量为![]() ,故D正确。故选B。
,故D正确。故选B。

练习册系列答案
相关题目