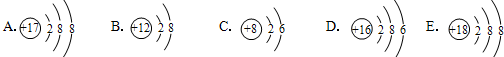题目内容
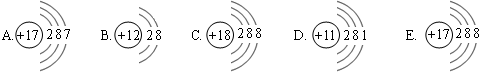
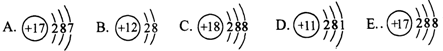
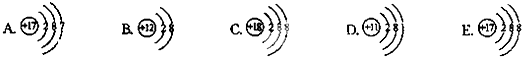
下面是五种粒子的结构示意图:
(1)图中粒子共能表示 种元素.A所表示的元素位于元素周期表的第 周期.
(2)图中表示的阳离子是 (用离子符号表示),表示的阴离子是 (用离子符号表示),二者形成的化合物的化学式为 .
【答案】分析:同种元素形成的粒子,质子数相同,原子呈电中性,对阳离子而言,核电荷数>核外电子数.如何找出原子和离子的区别,可以从质子数与核外电子的关系、粒子的带电性等方面加以考虑.原子的核外电子层数表示该元素所处的周期.
解答:解:(1)A与E核内质子数相同,表示同一种元素,所以共有4种元素.A原子核外有3个电子层,所以其表示的元素在第3周期.所以答案为:4;3.
(2)A、C和D中,核电荷数=核外电子数,表示原子,B中核电荷数>核外电子数,失去2个电子,表示阳离子,形成化合物时常显示+2价,质子数为12,所以该粒子表示镁离子,E中核电荷数<核外电子数,得到1个电子,表示阴离子,形成化合物时常显示-1价,质子数为17,所以该粒子表示氯离子,它们形成的化合物为氯化镁.所以答案为:Mg2+;Cl-;MgCl2.
点评:本题注重基础,考查知识点较多,并且题目难度不很大,对基础知识的掌握有很大帮助,多注重一些规律的记忆和积累.
解答:解:(1)A与E核内质子数相同,表示同一种元素,所以共有4种元素.A原子核外有3个电子层,所以其表示的元素在第3周期.所以答案为:4;3.
(2)A、C和D中,核电荷数=核外电子数,表示原子,B中核电荷数>核外电子数,失去2个电子,表示阳离子,形成化合物时常显示+2价,质子数为12,所以该粒子表示镁离子,E中核电荷数<核外电子数,得到1个电子,表示阴离子,形成化合物时常显示-1价,质子数为17,所以该粒子表示氯离子,它们形成的化合物为氯化镁.所以答案为:Mg2+;Cl-;MgCl2.
点评:本题注重基础,考查知识点较多,并且题目难度不很大,对基础知识的掌握有很大帮助,多注重一些规律的记忆和积累.

练习册系列答案
相关题目