题目内容
【题目】(每空1分,最后两小题各2分,共10分)
据有关资料介绍,儿童缺钙会得佝偻病,成年人缺钙会得软骨病,血液中也有少量钙,它对皮肤伤口血液的凝固起着重要作用。
(1)钙原子结构示意图如图所示,该原子的核电荷数为 ,它在元素周期表中位于第 周期;钙离子符号为 。
(2)钙元素的化学性质与下列哪种元素化学性质相似 ?
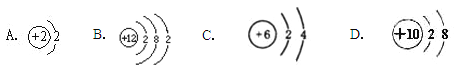
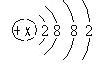
(3)若某粒子的结构示意图为
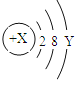
当X-Y=8时,该粒子的化学符号为 。
(4)市场上出现的某钙片的标签如图,经检验知,此钙片中含钙物质只有碳酸钙(CaCO3)。

①此标签中标注的含钙量是否合理? (填“合理”或“不合理” )
②如果一个青少年每天需补钙0.8克,其中有0.6克来自于牛奶及其他食品,其余服用钙片。请计算每天他需补充碳酸钙多少克?
③7.4克氢氧化钙[Ca(OH)2]与多少克碳酸钙[CaCO3]含钙元素质量相等?
【答案】(1)20 四 Ca2+
(2)B
(3)S2-
(4)①不合理 ②0.5克 ③10克
【解析】
试题分析:(1)在原子中,质子数=核电荷数=核外电子数,根据钙元素的原子示意图可知,它的核外电子数为20,故核电荷数为20;钙原子由4个电子层,故位于第四周期;钙原子的最外层电子数为2 ,易失去2个电子形成带2个单位正电荷的钙离子,根据离子的表示方法:在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,故钙离子表示为Ca2+;
(2)元素的化学性质与其最外层电子数关系密切,即最外层电子数相同的粒子具有相似的化学性质,由于钙元素的最外层电子数为2,故与化学性质相似的是最外层电子数同样是2的B;
(3)电子层数大于1时,最外层电子数为8时为稳定结构。故该粒子中,Y为8,根据X-Y=8,那么X=8+Y,故X=16,为硫元素,硫原子得到2个电子形成的是硫离子,表示为S2-;
(4)①碳酸钙中钙元素的质量分数=40/100 ×100%=40%。根据标签,100片钙片的的质量为80g,那么每片钙片的质量为0.8g,若钙片含的全部都是碳酸钙,那么0.8g碳酸钙中钙元素的质量=0.8g×40%=0.32g<0.75g,故此标签中标注的含钙量不合理;
②根据题意,那么通过服用钙片获得的钙元素的质量为0.8g-0.6g=0.2g;设每天他需补充碳酸钙的质量为x,那么:x ×40%=0.2g ,X=0.5g ;
③设7.4克氢氧化钙[Ca(OH)2]与质量为y碳酸钙[CaCO3]含钙元素质量相等,则:
7.4g×40/74 ×100% =40%y
Y=10g
答:略

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案【题目】某学习小组同学用过氧化氢溶液制取氧气。
(1)下表是分解等量的过氧化氢溶液时选用不同催化剂所得到的实验数据:
催化剂(质量均为0.3g) | 新鲜猪肝 | CuCl2 | MnO2 | CuO |
收集1L氧气所需的时间(s) | 42 | 650 | 18 | 300 |
从上述数据可得出一个结论: 。
(2)取含过氧化氢1.7g的溶液,加入适量MnO2充分反应(2H2O2![]() 2H2O+O2↑),请你根据化学方程式计算制取氧气的质量。
2H2O+O2↑),请你根据化学方程式计算制取氧气的质量。
【题目】下列对一些事实的解释错误的是
事 实 | 解 释 | |
A | 书写档案规定必须使用碳素墨水 | 常温下碳的化学性质稳定 |
B | 活性炭能去除河水中的异味 | 活性炭有吸附性 |
C | 焦炭可以把铁从它的氧化物矿石里还原出来 | 焦炭具有氧化性 |
D | 金刚石、石墨和 C60的物理性质差异很大 | 它们的原子排列方式不同 |