题目内容
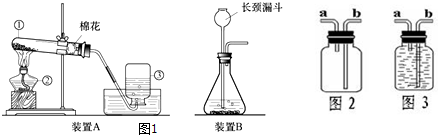
根据如图所示装置回答有关问题:
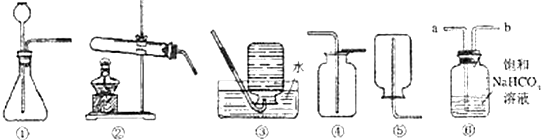
(1)写出图中标号仪器的名称:① ② ③ ④
(2)实验室制取二氧化碳,应选 (填序号,下同)作发生装置,实验室制取二氧化碳的化学方程式是 ;应选 作收集装置
(3)若实验室用装置⑥除去CO2气体中混有的少量氯化氢气体,不纯气体应从 (填a或b)导管通入.若要得到干燥纯净的CO2气体,按气流方向干燥装置应放于装置⑥之 (填前或后)
(4)若实验室用装置⑥检验CO2,则其中的药品应换成 .
(5实验室如果采用高锰酸钾制取O2并用排水法收集O2时,必须选用上述仪器中的 (填序号),反应化学方程式为 .
(6)氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3,同时得到氯化钙和水,该反应的化学方程式为 ,实验制取和收集NH3必须选用上述仪器中的 (填序号).

(1)写出图中标号仪器的名称:①
(2)实验室制取二氧化碳,应选
(3)若实验室用装置⑥除去CO2气体中混有的少量氯化氢气体,不纯气体应从
(4)若实验室用装置⑥检验CO2,则其中的药品应换成
(5实验室如果采用高锰酸钾制取O2并用排水法收集O2时,必须选用上述仪器中的
(6)氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3,同时得到氯化钙和水,该反应的化学方程式为
考点:常用气体的发生装置和收集装置与选取方法,气体的干燥(除水),实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据实验室常用仪器解答;
(2)制取二氧化碳采用的原料是碳酸钙和稀盐酸,所以写方程式时要注意.制取二氧化碳由于是固体和液体在不加热条件下进行,所以选用①装置来制取,由于二氧化碳溶解于水且密度比空气大,所以选用向上排空气法收集而选④;
(3)由于盐酸具有挥发性,随着反应的进行,收集的二氧化碳往往混有氯化氢气体,所以可以从洗气瓶将之除去,洗气瓶是长进短出.若获取干燥的气体,需要将干燥装置放在洗气装置之后,这样可以避免二次引入水蒸气;
(4)根据二氧化碳能使澄清的石灰水变浑浊解答;
(5)根据高锰酸钾制取氧气属于固固加热型,氧气不易溶于水解答,写出反应的方程式;
(6)根据实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3,同时得到氯化钙和水,写出反应的化学方程式;根据氨气(NH3)是一种密度比空气小,极易溶于水的气体选择收集方法.
(2)制取二氧化碳采用的原料是碳酸钙和稀盐酸,所以写方程式时要注意.制取二氧化碳由于是固体和液体在不加热条件下进行,所以选用①装置来制取,由于二氧化碳溶解于水且密度比空气大,所以选用向上排空气法收集而选④;
(3)由于盐酸具有挥发性,随着反应的进行,收集的二氧化碳往往混有氯化氢气体,所以可以从洗气瓶将之除去,洗气瓶是长进短出.若获取干燥的气体,需要将干燥装置放在洗气装置之后,这样可以避免二次引入水蒸气;
(4)根据二氧化碳能使澄清的石灰水变浑浊解答;
(5)根据高锰酸钾制取氧气属于固固加热型,氧气不易溶于水解答,写出反应的方程式;
(6)根据实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3,同时得到氯化钙和水,写出反应的化学方程式;根据氨气(NH3)是一种密度比空气小,极易溶于水的气体选择收集方法.
解答:解:
(1)根据实验室常用仪器可知是长颈漏斗;
(2)制取二氧化碳采用的原料是碳酸钙和稀盐酸,所以写方程式时要注意,方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
制取二氧化碳由于是固体和液体在不加热条件下进行,所以选用①装置来制取,由于二氧化碳溶解于水且密度比空气大,所以选用向上排空气法收集而选④.
(3)由于盐酸具有挥发性,随着反应的进行,收集的二氧化碳往往混有氯化氢气体,所以可以从洗气瓶将之除去,洗气瓶是长进短出.若获取干燥的气体,需要将干燥装置放在洗气装置之后,这样可以避免二次引入水蒸气.
(4)二氧化碳能使澄清的石灰水变浑浊,检验CO2,则其中的药品应换成澄清的石灰水;
(5)高锰酸钾制取氧气属于固固加热型,氧气不易溶于水,必须选用上述仪器中的②和③,该反应的化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑
(6)实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3,同时得到氯化钙和水,反应的化学方程式为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O 氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验制取和收集NH3必须选用上述仪器中的②和⑤
答案:
(1)长颈漏斗、酒精灯、水槽、集气瓶
(2)①CaCO3+2HCl═CaCl2+H2O+CO2↑ ④
(3)a 后
(4)澄清的石灰水
(5)②和③2KMnO4
K2MnO4+MnO2+O2↑
(6)Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O ②和⑤
(1)根据实验室常用仪器可知是长颈漏斗;
(2)制取二氧化碳采用的原料是碳酸钙和稀盐酸,所以写方程式时要注意,方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
制取二氧化碳由于是固体和液体在不加热条件下进行,所以选用①装置来制取,由于二氧化碳溶解于水且密度比空气大,所以选用向上排空气法收集而选④.
(3)由于盐酸具有挥发性,随着反应的进行,收集的二氧化碳往往混有氯化氢气体,所以可以从洗气瓶将之除去,洗气瓶是长进短出.若获取干燥的气体,需要将干燥装置放在洗气装置之后,这样可以避免二次引入水蒸气.
(4)二氧化碳能使澄清的石灰水变浑浊,检验CO2,则其中的药品应换成澄清的石灰水;
(5)高锰酸钾制取氧气属于固固加热型,氧气不易溶于水,必须选用上述仪器中的②和③,该反应的化学方程式为:2KMnO4
| ||
(6)实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3,同时得到氯化钙和水,反应的化学方程式为:Ca(OH)2+2NH4Cl
| ||
答案:
(1)长颈漏斗、酒精灯、水槽、集气瓶
(2)①CaCO3+2HCl═CaCl2+H2O+CO2↑ ④
(3)a 后
(4)澄清的石灰水
(5)②和③2KMnO4
| ||
(6)Ca(OH)2+2NH4Cl
| ||
点评:常见气体的制取是化学实验考查的基础和常见的形式,在回答时一定要注意因果关系的对应,同时注意语言描述要准确到位.多功能瓶的使用是“洗气瓶是长进短出,储气瓶是短进长出”.

练习册系列答案
相关题目
下列常见物质在生活中使用不当的是( )
| A、做馒头时用纯碱中和发酵中产生的酸 |
| B、铁锈通常用稀盐酸洗去 |
| C、酸雨侵蚀后的土壤通常播撒熟石灰 |
| D、治疗胃酸过多的药物中通常含有氢氧化钠 |
 ”表示A原子,“
”表示A原子,“ ”表示B原子,“
”表示B原子,“ ”表示C原子,在点燃条件下,每四个甲分子能与三个乙分子反应,生成两个丙分子和六个丁分子.从微观角度回答下列问题:
”表示C原子,在点燃条件下,每四个甲分子能与三个乙分子反应,生成两个丙分子和六个丁分子.从微观角度回答下列问题: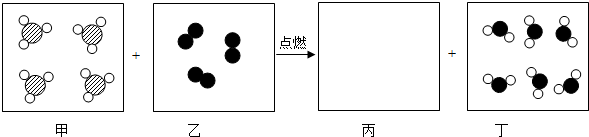
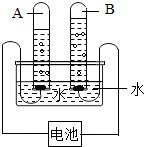 生活离不开水,净化水的知识在日常生活中有着广泛的应用
生活离不开水,净化水的知识在日常生活中有着广泛的应用