题目内容
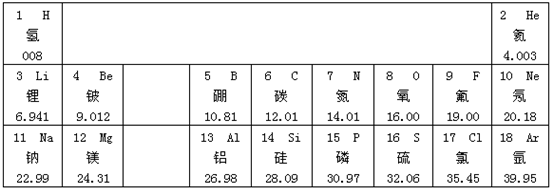
(1)可从表中查得氟原子的相对原子质量是
(2)从周期表中,可以判断出元素间的本质区别是
A.质子数 B.中子数 C.电子数
(3)最外层电子数也称价电子数,对非金属元素可确定最高化合价和最低化合价:
①画出7号元素原子的核外电子排布
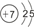
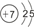
②7号元素的最低化合价与氢元素形成化合物的化学式是
(2)根据元素的不同与质子数的关系完成
(3)①根据在原子中核外电子排布规律完成;②根据7号元素的最外层电子数分析其化合价并书写化学式即可.
(2)不同元素的本质区别是质子数或核电荷数不同
(3)①根据在原子中核外电子排布规律可知7号原子核外电子排布规律是第一层有两个电子,第二层有5个电子;②根据7号元素的最外层电子数5,易得到3个电子而形成8个电子的稳定结构,可知其最低的负价是-3价,而氢元素的化合价一般为+1价,所以7号元素的最低化合价与氢元素形成化合物的化学式NH3.
故答案为:(1)19.(2)A.(3)①
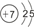 ; ②NH3.
; ②NH3.
元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
|
族
周期 |
I A |
II A |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 炭 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
3 |
11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
(1)请从上表中查出关于硼元素的一条信息:___________________________。
(2)请从上表中找出一种元素名称是错误的,更正为 .
(3)第3周期(横行)中属于金属元素的是 (填一种元素符号),其阳离子是 。
(4)在金属活泼性中,镁元素比铝元素活泼,请你从原子结构的观念进行解释 。
(5)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻, 其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体(SiF4)和水,该反应的化学方程式为 。
元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
|
|
I A |
II A |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
3 |
11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
(1)请从上表中查出关于硼元素的一条信息: 。
(2)第3周期中相对原子质量最大的金属元素的是 。
(3)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是 (填标号)。
a.C和Ne b.Be和Mg c.Al和Si d.F和Cl
(4)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻,其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体和水,该反应的化学方程式为 。