题目内容
化学实验室常用甲酸(一种液态物质,化学式为HCOOH)和浓硫酸混合加热制备一氧化碳,其反应方程式为:HCOOH
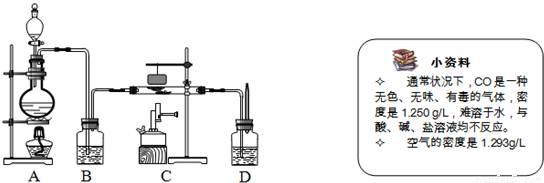
CO↑+H2O.如图是制备CO,再用CO还原氧化铁并检验反应产物的实验装置.
(1)根据“小资料”中的内容分析:如果实验室想收集CO气体,你认为用何种方法比较好
A.排水收集法 B.向上排空气法 C.向下排空气法 D.排水法和向下排空气法均可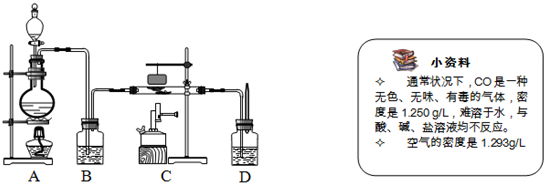
(2)实验前先检查
(3)为了使实验能顺利进行,装置B中盛放
装置D中盛放
(4)实验结束时应先停止
(5)反应后将磁铁悬挂在玻璃管上方,其作用是
(6)写出C中硬质玻璃管中发生化学反应的方程式
| 浓H2SO4 |
| △ |
(1)根据“小资料”中的内容分析:如果实验室想收集CO气体,你认为用何种方法比较好
A
A
.(填字母代号)A.排水收集法 B.向上排空气法 C.向下排空气法 D.排水法和向下排空气法均可

(2)实验前先检查
装置气密性
装置气密性
;实验C处,实验前应检验检验CO的纯度并驱除尽装置内的空气
检验CO的纯度并驱除尽装置内的空气
,以防爆炸.(3)为了使实验能顺利进行,装置B中盛放
浓硫酸
浓硫酸
(填名称);装置D中盛放
澄清石灰水
澄清石灰水
(填溶液名称),以检验CO2
CO2
;(4)实验结束时应先停止
C
C
处加热(填字母代号).(5)反应后将磁铁悬挂在玻璃管上方,其作用是
将铁从混合物中分离出来
将铁从混合物中分离出来
.(6)写出C中硬质玻璃管中发生化学反应的方程式
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
分析:(1)根据气体的密度、溶解性选择收集装置;
(2)根据实验注意事项分析,一氧化碳具有可燃性,与空气或氧气混合达到一定程度时遇明火会发生爆炸;
(3)浓硫酸具有吸水性,可以用作干燥剂;二氧化碳能使石灰水变浑浊;
(4)根据实验注意事项分析;
(5)根据磁铁能够吸引铁分析;
(6)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
(2)根据实验注意事项分析,一氧化碳具有可燃性,与空气或氧气混合达到一定程度时遇明火会发生爆炸;
(3)浓硫酸具有吸水性,可以用作干燥剂;二氧化碳能使石灰水变浑浊;
(4)根据实验注意事项分析;
(5)根据磁铁能够吸引铁分析;
(6)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
解答:解:(1)根据小资料可知一氧化碳的密度比空气略小,不能用向下排空气法收集,难溶于水,因此可用排水法收集;
(2)实验前先检查装置的气密性,以防生成的气体外逸;因为一氧化碳和空气或氧气混合达到一定程度时遇明火会发生爆炸,所以开始应该检验CO的纯度并驱除尽装置内的空气,以防止爆炸;
(3)浓硫酸具有吸水性,可以除去一氧化碳中的水蒸气,因此B中应盛放浓硫酸;石灰水遇二氧化碳变浑浊,可以用石灰水检验二氧化碳,因此D中盛放澄清的石灰水;
(4)实验结束时应先停止C处的加热,继续通入一氧化碳直到玻璃管冷却,这样可以防止高温下铁被空气中的氧气氧化;
(5)磁铁能够吸引铁,可以把铁和其它物质组成的混合物分离,从而得到铁;
(6)氧化铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式为:3CO+Fe2O3
2Fe+3CO2.
故答案为:(1)A;(2)装置气密性;检验CO的纯度并驱除尽装置内的空气;(3)浓硫酸;澄清石灰水; CO2;(4)C;(5)将铁从混合物中分离出来; (6)3CO+Fe2O3
2Fe+3CO2.
(2)实验前先检查装置的气密性,以防生成的气体外逸;因为一氧化碳和空气或氧气混合达到一定程度时遇明火会发生爆炸,所以开始应该检验CO的纯度并驱除尽装置内的空气,以防止爆炸;
(3)浓硫酸具有吸水性,可以除去一氧化碳中的水蒸气,因此B中应盛放浓硫酸;石灰水遇二氧化碳变浑浊,可以用石灰水检验二氧化碳,因此D中盛放澄清的石灰水;
(4)实验结束时应先停止C处的加热,继续通入一氧化碳直到玻璃管冷却,这样可以防止高温下铁被空气中的氧气氧化;
(5)磁铁能够吸引铁,可以把铁和其它物质组成的混合物分离,从而得到铁;
(6)氧化铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式为:3CO+Fe2O3
| ||
故答案为:(1)A;(2)装置气密性;检验CO的纯度并驱除尽装置内的空气;(3)浓硫酸;澄清石灰水; CO2;(4)C;(5)将铁从混合物中分离出来; (6)3CO+Fe2O3
| ||
点评:本题考查了基本实验的设计,难度不大,注意该实验起始时一定检验CO的纯度,否则可能有安全事故发生.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
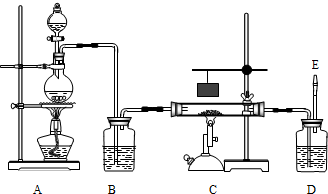
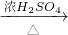 CO↑+H2O.如图是制备一氧化碳还原三氧化二铁并检验反应产物结束时的实验装置.
CO↑+H2O.如图是制备一氧化碳还原三氧化二铁并检验反应产物结束时的实验装置.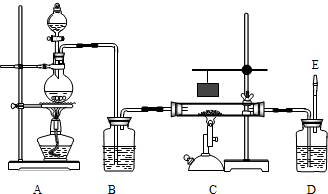
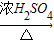 CO↑+H2O.如图是制备CO,再用CO还原氧化铁并检验反应产物的实验装置.
CO↑+H2O.如图是制备CO,再用CO还原氧化铁并检验反应产物的实验装置.