题目内容
【题目】某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A﹣H编号后,做如下实验。
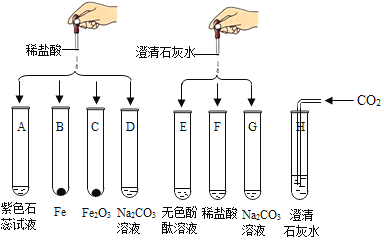
(1)实验中观察到有气泡出现的试管是_____、_____,有沉淀生成的试管是_____、_____。
(2)写出实验中无明显现象产生的试管中发生的化学方程式_____。
(3)实验后某试管中为红色溶液,当向其中加入过量的_____后,溶液变为蓝色。由此推断,该试管中最初盛有的物质是_____。
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是_____、_____。
(5)写出此实验试管中发生反应的化学方程式
试管C中_____,试管D中_____,试管H中_____。
【答案】B D G H Ca(OH)2+2HCl═CaCl2+2H2O 氢氧化钠溶液 紫色石蕊试液 氢氧化钠 碳酸钠 Fe2O3+6HCl═2FeCl3+3H2O Na2CO3+2HCl═2NaCl+H2O+CO2↑ Ca(OH)2+CO2═CaCO3↓+H2O
【解析】
(1)实验中,B中铁和盐酸反应生成氢气,D中碳酸钠和盐酸反应生成二氧化碳,G中碳酸钠和氢氧化钙反应生成碳酸钙沉淀,H中二氧化碳和氢氧化钙反应生成碳酸钙沉淀,因此观察到有气泡出现的试管是B、D,有沉淀生成的试管是G、H。故填:B;D;G;H
(2)实验中无明显现象产生的试管是F,氢氧化钙和盐酸反应生成氯化钙和水,发生的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O。故填:Ca(OH)2+2HCl═CaCl2+2H2O
(3)实验后A试管中为红色溶液,当向其中加入过量的氢氧化钠溶液后,溶液显碱性,溶液变为蓝色,A试管中最初盛有的物质是紫色石蕊试液。故填:氢氧化钠溶液;紫色石蕊试液
(4)实验后G试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,是因为盐酸先和氢氧化钠反应生成氯化钠和水,后和碳酸钠反应生成氯化钠、水和二氧化碳,则该滤液中的溶质是反应生成的氢氧化钠和过量的碳酸钠。故填:氢氧化钠;碳酸钠
(5)试管C中氧化铁和盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;试管D中盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;试管H中氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O。故填:Fe2O3+6HCl═2FeCl3+3H2O;Na2CO3+2HCl═2NaCl+H2O+CO2↑;Ca(OH)2+CO2═CaCO3↓+H2O