题目内容
取某碳酸钠样品50g(含氯化钠和13%的不溶性杂质,杂质不参加化学反应),放入质量为200g的烧杯中,加137.7g水充分溶解,再向烧杯中加入300g稀盐酸恰好完全反应,测得反应后烧杯与烧杯内物质的总质量为674.5g。求所得溶液中溶质的质量分数。
解:生成二氧化碳气体的质量为
50g+200g+137.7g+300g-674.5g=13.2g
设样品中含碳酸钠的质量为x,反应后生成的氯化钠的质量为y
Na2CO3 + 2HCl = 2NaCl + H2O+ CO2↑
106 117 44
x y 13.2g
|
 =
= x=31.8g
x=31.8g
 =
=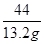 y=35.1g
y=35.1g
所得溶液中的溶质为 35.1g+(50g-31.8g-50g×13%)=46.8g
|
NaCl%= = 10%
= 10%
答:反应后溶液中溶质的质量分数为10%。
解析:略

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目