题目内容
【题目】“侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠.某化学兴趣小组的同学拟测定某纯碱样品中Na2CO3的质量分数. 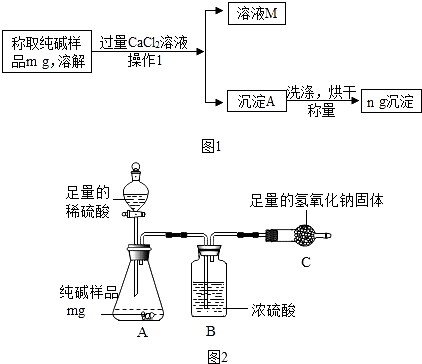
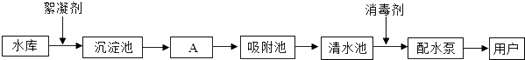
【方案一】沉淀分析法(如图1所示)则:
(1)“操作Ⅰ”的名称是 .
(2)溶液M中含有的阳离子有 .
(3)确定CaCl2溶液是否过量的方法是 .
A.静置混合物,向上层清液中再滴加CaCl2溶液,如果无沉淀,则过量
B.向溶液M中滴加CaCl2溶液,如果有沉淀,则过量
(4)若沉淀A没有洗涤烘干,导致Na2CO3的质量分数(填“偏大”、“偏小”或“不变”).判断沉淀A洗净的方法是:取最后一次洗涤所得滤液,滴加AgNO3溶液,若(填“有”或“无”)白色沉淀,则洗涤干净.
(5)样品中Na2CO3的质量分数为(用字母m、n的代数式表示).
(6)【方案二】气体分析法(如图2所示) A装置中反应的化学方程式为 , 盛稀硫酸的仪器名称为 .
(7)B装置的作用是;C装置中反应的化学方程式为
(8)通过称量装置在反应前后的质量,即可求得产生二氧化碳的质量.
(9)理论上【方法二】比【方案一】会产生较大的误差,原因是 .
【答案】
(1)过滤
(2)钠离子和钙离子
(3)A
(4)偏大;无
(5)![]()
(6)Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;分液漏斗
(7)除去水蒸气;CO2+2NaOH=Na2CO3+H2O
(8)C
(9)装置内的残留二氧化碳没有被吸收,空气中的二氧化碳和水蒸气也会进入C装置
【解析】解:【方案一】(1)“操作Ⅰ”的名称是过滤. 所以答案是:过滤;(2)样品中的氯化钠和氯化钙不反应,由于氯化钙过量,因此碳酸钠完全反应,且生成了氯化钠,因此溶液M中含有的阳离子有钠离子和钙离子.
所以答案是:钠离子和钙离子;(3)若CaCl2不过量,则会有Na2CO3剩余,再加入CaCl2后若生成沉淀则说明不过量,如果无沉淀,则过量,故选A;(4)若沉淀A没有洗涤烘干,会导致计算出的碳酸钠质量偏大,碳酸钠的质量分数就偏大;判断沉淀A洗净的方法是:取最后一次洗涤所得滤液,滴加AgNO3溶液,若无白色沉淀,则洗涤干净.
所以答案是:偏大;无;(5)设样品中Na2CO3的质量分数为x,则
Na2CO3+CaCl2=2NaCl+ | CaCO3↓ |
106 | 100 |
mgx | ng |
![]() =
= ![]() ,解得x=
,解得x= ![]() .
.
所以答案是: ![]() ;
;
【方案二】(1)碳酸钠和稀硫酸反应的化学方程式为Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,盛稀硫酸的仪器名称为分液漏斗.
所以答案是:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;分液漏斗;(2)浓硫酸具有吸水性,因此B装置的作用是除去水蒸气;二氧化碳和氢氧化钠反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
所以答案是:除去水蒸气;CO2+2NaOH=Na2CO3+H2O;(3)C装置在反应前后的质量差,即是产生二氧化碳的质量.
所以答案是:C;(4)【方法二】中装置内的残留二氧化碳没有被吸收,空气中的二氧化碳和水蒸气也会进入C装置.
所以答案是:装置内的残留二氧化碳没有被吸收,空气中的二氧化碳和水蒸气也会进入C装置;
【考点精析】解答此题的关键在于理解过滤操作的注意事项的相关知识,掌握过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损,以及对书写化学方程式、文字表达式、电离方程式的理解,了解注意:a、配平 b、条件 c、箭号.

【题目】下表是元素周期表的一部分:
族 | IA | 0 | ||||||
一 | 1H | ⅡA | ⅢA | ⅣA | V A | ⅥA | ⅦA | 2He |
二 | 3Li | 4Be | 5B | 6C | 7N | 8O | 9F | 10Ne |
三 | 11Na | 12Mg | 13Al | 14Si | 15P | 16S | 17Cl | 18Ar |
(1)12号元素的元素名称为;Be元素的相对原子质量为 .
(2)相对原子质量为28.09的元素属元素(填“金属”或“非金属”);Ne的化学性质;O与S元素化学性质相似的原因为 .
(3)表中不同种元素最本质的区别是(填字母).
A.质子数不同
B.相对原子质量不同
C.中子数不同
(4)如图所示为某元素的原子结构示意图,该元素位于周期表中第周期. 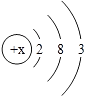
(5)从11 Na~18 Ar你可总结出的一条规律是