题目内容
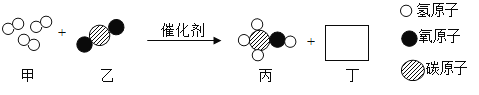
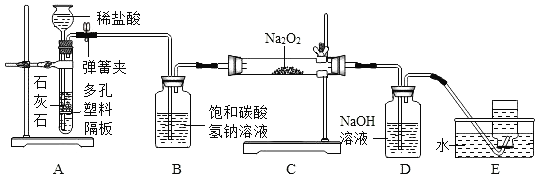
【题目】探究学习小组在实验室中用如图所示装置制取CO2,探究CO2与过氧化钠(Na2O2)的反应,并收集纯净的氧气。
查阅资料得知:过氧化钠(Na2O2)是一种淡黄色固体,能与CO2、H2O发生反应:2Na2O2+2CO2=2Na2CO3+O2, 2Na2O2+2H2O=4NaOH+O2↑。
请回答下列问题:
(1)利用装置A制取CO2的优点是____。
(2)装置B的作用是吸收CO2中混有的HCl气体,发生反应的化学方程式______。
(3)装置D的作用是_____。
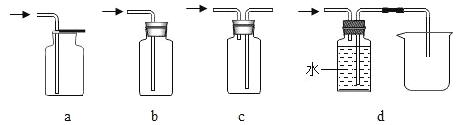
(4)装置E中收集到的气体是_____(填化学式),该气体还可以用下列装置中的_____(填写字母序号)进行收集。
(5)为探究反应后装置C硬质玻璃管中固体的成分,该小组同学进行了下列实验:
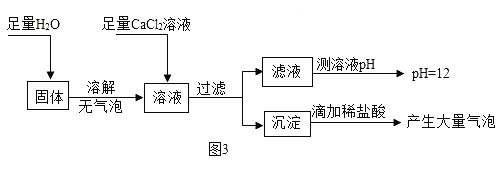
根据实验判断反应后装置C硬质玻璃管中的固体为_____。
【答案】便于控制反应的发生和停止 NaHCO3+HCl=NaCl+H2O+CO2↑ 除去二氧化碳气体 O2 ad 氢氧化钠和碳酸钠
【解析】
(1)利用装置A制取CO2的优点是能使反应随时进行或停止,原理是:关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止;打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行;
(2)装置B的作用是吸收CO2中混有的HCl,碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,发生反应的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑;
(3)装置D的作用是吸收没有反应的二氧化碳气体;
(4)装置E中收集的氧气还可以用下列图2装置中的a、d装置,这是因为氧气密度比空气大,可以用向上排空气法收集,不易溶于水,可以用排水法收集,即可以用ad装置收集;
(5)固体溶解不产生气泡,说明固体中不含有过氧化钠,加入足量氯化钙溶液后,溶液pH=12,显碱性,说明溶液中含有氢氧化钠,沉淀和稀盐酸反应生成气体,说明固体中含有碳酸钠,因此反应后装置C硬质玻璃管中固体是Na2CO3、NaOH。

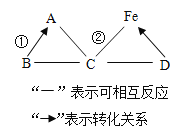
【题目】甲、乙、内三种物质的转化关系见下面如图所示,“→”表示反应可以一步实现(部分物质和反应条件已省略),下面选项中不能按图示转化关系实现的是( )
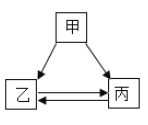
选项 | 甲 | 乙 | 丙 |
A | H2SO4 | H2 | H2O |
B | NaOH | NaCl | NaNO3 |
C | Na2O | NaOH | Na2CO3 |
D | Ca(OH)2 | CaCl2 | CaCO3 |
A. AB. BC. CD. D