题目内容
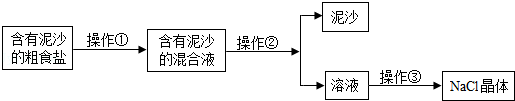
通过海水晒制可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质。以下是制备精盐的实验方案:
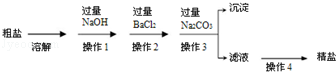
回答下列问题:
(1)操作1中,加入NaOH溶液除杂时,反应的化学方程式为 ; 。
(2)操作2中,不能用硝酸钡溶液代替BaCl2溶液,原因是 。
(3)加入Na2CO3除去的杂质离子是 。
(4)进行操作3后,判断Na2CO3过量的方法是 。
(5)滤液中,需加入适量的试剂,这种试剂的名称是 。
(6)在操作4中,需要进行蒸发,蒸发时需用到的仪器有铁架台(含铁圈)、酒精灯、玻璃棒、 。
(7)若精盐的产率偏低,可能的原因是 。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解粗盐时,加入的水量不足,粗盐没有完全溶解

回答下列问题:
(1)操作1中,加入NaOH溶液除杂时,反应的化学方程式为 ; 。
(2)操作2中,不能用硝酸钡溶液代替BaCl2溶液,原因是 。
(3)加入Na2CO3除去的杂质离子是 。
(4)进行操作3后,判断Na2CO3过量的方法是 。
(5)滤液中,需加入适量的试剂,这种试剂的名称是 。
(6)在操作4中,需要进行蒸发,蒸发时需用到的仪器有铁架台(含铁圈)、酒精灯、玻璃棒、 。
(7)若精盐的产率偏低,可能的原因是 。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解粗盐时,加入的水量不足,粗盐没有完全溶解
(1)2NaOH+MgCl2=Mg(OH)2↓+2NaCl、MgSO4+2NaOH=Mg(OH)2↓+Na2SO4
(2)引入了杂质硝酸钠 (3)Ca2+、Ba2+(4)少量滤液于试管中,滴加稀盐酸,有气泡产生
(5)稀盐酸 (6)蒸发皿 (7)B、C
(2)引入了杂质硝酸钠 (3)Ca2+、Ba2+(4)少量滤液于试管中,滴加稀盐酸,有气泡产生
(5)稀盐酸 (6)蒸发皿 (7)B、C
试题分析:(1)氢氧化钠能和氯化镁、硫酸镁反应分别生成氢氧化镁和氯化钠、氢氧化镁和硫酸钠,反应的化学方程式分别为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl、MgSO4+2NaOH=Mg(OH)2↓+Na2SO4。
(2)不能用硝酸钡溶液代替BaCl2溶液,如果是加入硝酸钡溶液,经过一系列反应后,最后得到的氯化钠中会含有硝酸钠,故填:引入了杂质硝酸钠。
(3)加入Na2CO3可以除去的杂质离子是钙离子和钡离子,故填:Ca2+、Ba2+。
(4)判断Na2CO3过量的方法是:取少量滤液于试管中,滴加稀盐酸,有气泡产生,故填:取少量滤液于试管中,滴加稀盐酸,有气泡产生。
(5)滤液中,如果加入适量的稀盐酸,会与其中的氢氧化钠、碳酸钠反应分别生成氯化钠和水、氯化钠、水和二氧化碳,从而得到氯化钠溶液,故填:稀盐酸。
(6)蒸发时需用到的仪器有铁架台(含铁圈)、酒精灯、玻璃棒、蒸发皿,故填:蒸发皿。
(7)A.过滤时滤纸有破损,能使精盐的产率偏高;B.蒸发时有固体溅出,能使精盐的产率偏低;C.溶解粗盐时,加入的水量不足,粗盐没有完全溶解,能使精盐的产率偏低,故填:B、C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
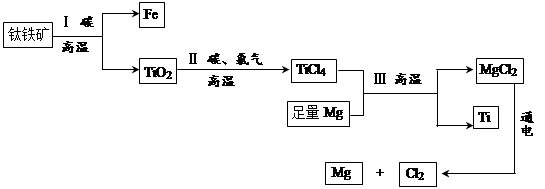
 ),则可能的原因是(填字母) .
),则可能的原因是(填字母) .