题目内容
【题目】有一包白色粉末可能由NaCl、NaNO3、MgCl2、CuSO4中的一种或多种物质组成,小明为了探究其成分,设计并完成了如图所示的实验. 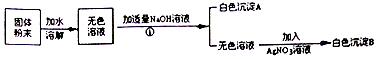
根据以上实验,回答:
(1)请写出操作①的名称 .
(2)原固体粉末中一定不含有什么物质? .
(3)请写出生成沉淀A的化学方程式 .
【答案】
(1)过滤
(2)硫酸铜
(3)MgCl2+2NaOH=Mg(OH)2↓+2NaCl
【解析】解:硫酸铜在溶液中显蓝色,氯化镁和氢氧化钠反应会生成白色的氢氧化镁沉淀,氯离子和银离子反应会生成白色的氯化银沉淀,所以 固体粉末加水溶解,得到无色溶液,白色粉末中一定不含硫酸铜,无色溶液中加入氢氧化钠生成白色沉淀A,固体粉末中一定含有氯化镁,无色溶液中加入硝酸银会生成白色沉淀B,所以B是氯化银沉淀,氯化镁中也会提供氯离子,所以不能确定固体粉末中是否含有氯化钠,题中的现象也不能确定是否含有硝酸钠,所以(1)操作①的名称过滤;(2)原固体粉末中一定不含硫酸铜;(3)生成沉淀A的反应是氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
所以答案是:(1)过滤;(2)硫酸铜;(3)MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号才能正确解答此题.

练习册系列答案
相关题目