题目内容
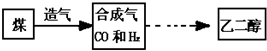
我国具有较丰富的煤炭资源,煤制取乙二醇的产业化发展是煤综合利用的方向.煤制取乙二醇的流程示意图为:
(1)煤属于______ (填“可再生”或“不可再生”)能源.
(2)合成气具有还原性,写出CO还原氧化铜的化学方程式:______,该化学反应中属于还原剂的物质是______.
(3)合成制取乙二醇的化学反应方程式为:2CO+3H2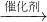 C2H6O2,该化学反应的基本类型是______;从得氧失氧的角度分析,该反应也是氧化还原反应,其中属于氧化剂的物质是______.
C2H6O2,该化学反应的基本类型是______;从得氧失氧的角度分析,该反应也是氧化还原反应,其中属于氧化剂的物质是______.
(4)根据对(2)与(3)的分析,你对CO的性质有什么新的认识?______.
(5)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质.仅用合成气为原料不可能得到的物质是______ (填字母序号).
a.草酸(HOOCCOOH) b.甲醇(CH3OH) c.尿素[CO(NH2)2].
解:(1)煤属于不可再生能源;
(2)氧化铜和一氧化碳在加热的条件下生成铜和二氧化碳,反应的化学方程式:CO+CuO Cu+CO2;其中一氧化碳化合价升高,属于还原剂;
Cu+CO2;其中一氧化碳化合价升高,属于还原剂;
(3)合成制取乙二醇的化学反应方程式为:2CO+3H2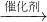 C2H6O2,该反应中反应物为两种,生成物是一种,符合化合反应的含义,其中一氧化碳得到氧,属于氧化剂;
C2H6O2,该反应中反应物为两种,生成物是一种,符合化合反应的含义,其中一氧化碳得到氧,属于氧化剂;
(4)根据对(2)与(3)的分析,一氧化碳具有还原性,有时也具有氧化性;
(5)根据质量守恒定律可知,化学反应前后元素的种类不变,合成气(CO和H2)在不同催化剂的作用下,合成的物质含有碳元素、氢元素和氧元素,不可能含有氮元素,不可能得到的物质是尿素,同样HOOCCOOH 的C:O=1:2,而 CO中 C:O=1:1,不可能出现1:2,所以也不可能合成.
故答案为:(1)不可再生;(2)CO+CuO Cu+CO2;CO;(3)化合反应;CO;(4)具有还原性,有时也具有氧化性;(5)ac.
Cu+CO2;CO;(3)化合反应;CO;(4)具有还原性,有时也具有氧化性;(5)ac.
分析:(1)根据化石燃料属于不可再生能源进行解答;
(2)根据氧化铜和一氧化碳在加热的条件下生成铜和二氧化碳进行解答;
(3)乙醇具有可燃性,可以推测乙二醇也具有可燃性;
(4)根据一氧化碳的性质进行解答;
(5)根据化学变化遵循质量守恒定律进行解答.
点评:解答本题要掌握化石燃料的性质,掌握化学方程式的书写方法,充分理解化学在社会发展中的作用,只有这样才能对问题做出正确的判断.
(2)氧化铜和一氧化碳在加热的条件下生成铜和二氧化碳,反应的化学方程式:CO+CuO
 Cu+CO2;其中一氧化碳化合价升高,属于还原剂;
Cu+CO2;其中一氧化碳化合价升高,属于还原剂;(3)合成制取乙二醇的化学反应方程式为:2CO+3H2
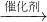 C2H6O2,该反应中反应物为两种,生成物是一种,符合化合反应的含义,其中一氧化碳得到氧,属于氧化剂;
C2H6O2,该反应中反应物为两种,生成物是一种,符合化合反应的含义,其中一氧化碳得到氧,属于氧化剂;(4)根据对(2)与(3)的分析,一氧化碳具有还原性,有时也具有氧化性;
(5)根据质量守恒定律可知,化学反应前后元素的种类不变,合成气(CO和H2)在不同催化剂的作用下,合成的物质含有碳元素、氢元素和氧元素,不可能含有氮元素,不可能得到的物质是尿素,同样HOOCCOOH 的C:O=1:2,而 CO中 C:O=1:1,不可能出现1:2,所以也不可能合成.
故答案为:(1)不可再生;(2)CO+CuO
 Cu+CO2;CO;(3)化合反应;CO;(4)具有还原性,有时也具有氧化性;(5)ac.
Cu+CO2;CO;(3)化合反应;CO;(4)具有还原性,有时也具有氧化性;(5)ac.分析:(1)根据化石燃料属于不可再生能源进行解答;
(2)根据氧化铜和一氧化碳在加热的条件下生成铜和二氧化碳进行解答;
(3)乙醇具有可燃性,可以推测乙二醇也具有可燃性;
(4)根据一氧化碳的性质进行解答;
(5)根据化学变化遵循质量守恒定律进行解答.
点评:解答本题要掌握化石燃料的性质,掌握化学方程式的书写方法,充分理解化学在社会发展中的作用,只有这样才能对问题做出正确的判断.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目