题目内容
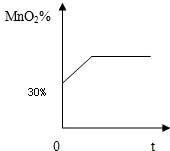 实验室用加热氯酸钾与二氧化锰混合物的方法来制取氧气,在制取过程中,固体中二氧化锰的质量分数(MnO2%)随加热时间(t)的变化情况如图.当二氧化锰的质量分数为多少时不再产生氧气( )
实验室用加热氯酸钾与二氧化锰混合物的方法来制取氧气,在制取过程中,固体中二氧化锰的质量分数(MnO2%)随加热时间(t)的变化情况如图.当二氧化锰的质量分数为多少时不再产生氧气( )| A、37.6% | B、42.2% | C、41.3% | D、53.8% |
分析:由于反应开始时二氧化锰的质量分数为30%,所以可假设开始氯酸钾和二氧化锰的质量之和100g,那么氯酸钾的质量为70g,然后根据氯酸钾受热分解的方程式,利用氯酸钾的质量求出反应后生成氯化钾的质量,进而求出反应后二氧化锰的质量分数.
解答:解:假设反应前混合物的质量为100g,则二氧化锰的质量为30g,氯酸钾的质量为70g.
设70g氯酸钾完全反应生成氯化钾的质量为x
2KClO3
2KCl+3O2↑
245 149
70g x
=
x=42.6g
所以反应后二氧化锰的质量分数为:
×100%=41.3%
故选C
设70g氯酸钾完全反应生成氯化钾的质量为x
2KClO3
| ||
| △ |
245 149
70g x
| 245 |
| 149 |
| 70g |
| x |
所以反应后二氧化锰的质量分数为:
| 30g |
| 30g+42.6g |
故选C
点评:此题是利用化学方程式的计算,此题没给任何物质质量的具体数值,给此题的计算加深了难度.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目