题目内容
(1)苯是一种强烈的至癌物,是新装修房子的室内污染物之一.其燃烧的化学方程式为:2X+15O2
| ||
(2)工业制取硫酸,主要用黄铁矿(主要成分:FeS2)作原料,在高温条件下与空气中的氧气反应,产生一种能形成酸雨的气体和一种铁锈主要成分的物质.该反应的化学方程式为:
分析:(1)根据燃烧的化学方程式为:2X+15O2
12CO2+6H2O,利用质量守恒定律来解答;
(2)根据信息来确定反应物和生成物,进一步来书写化学方程式.
| ||
(2)根据信息来确定反应物和生成物,进一步来书写化学方程式.
解答:解:(1)由燃烧的化学方程式为:2X+15O2
12CO2+6H2O,
根据质量守恒定律可知反应前后元素的种类、原子个数前后相等,
O原子个数前后相等,
由元素守恒可知,X中一定含有C、H元素,
由原子守恒可知,反应后共24个C原子、12个H原子,
又X的化学计量数为2,则X的化学式为C6H6,故答案为:C6H6.
(2)由FeS2在高温条件下与空气中的氧气反应,产生一种能形成酸雨的气体和一种铁锈主要成分的物质,
由元素守恒,则该能形成酸雨的气体应为二氧化硫,铁锈主要成分的物质为三氧化二铁,即FeS2和氧气反
应生成二氧化硫和三氧化二铁,故答案为:4FeS2+11O2
2Fe2O3+8SO2.
| ||
根据质量守恒定律可知反应前后元素的种类、原子个数前后相等,
O原子个数前后相等,
由元素守恒可知,X中一定含有C、H元素,
由原子守恒可知,反应后共24个C原子、12个H原子,
又X的化学计量数为2,则X的化学式为C6H6,故答案为:C6H6.
(2)由FeS2在高温条件下与空气中的氧气反应,产生一种能形成酸雨的气体和一种铁锈主要成分的物质,
由元素守恒,则该能形成酸雨的气体应为二氧化硫,铁锈主要成分的物质为三氧化二铁,即FeS2和氧气反
应生成二氧化硫和三氧化二铁,故答案为:4FeS2+11O2
| ||
点评:本题考查利用化学方程式来确定物质的化学式及利用物质来书写化学方程式,学生应注意利用元素守恒、原子守恒来分析解答问题,培养良好的学科思维方法.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
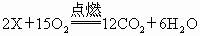 ,则X的化学式为:________.
,则X的化学式为:________.
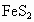 )作原料,在高温条件下与空气中的氧气反应,产生一种能形成酸雨的气体和一种铁锈主要成分的物质.该反应的化学方程式为:___________________________.
)作原料,在高温条件下与空气中的氧气反应,产生一种能形成酸雨的气体和一种铁锈主要成分的物质.该反应的化学方程式为:___________________________. 12CO2+6H2O,则X的化学式为:______.
12CO2+6H2O,则X的化学式为:______. 12CO2+6H2O,则X的化学式为:.
12CO2+6H2O,则X的化学式为:.