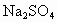题目内容
有
A、B、C三种物质,已知A为钠盐,B为氯化物,C为碱.经下列实验操作,其实验现象如下:①
A、B的溶液混合后无沉淀或气体产生;②
B、C的溶液混合后出现蓝色沉淀;③
A、C的溶液混合后出现白色沉淀,该沉淀不溶于稀硝酸.则
A为__________,B为_________,C为___________(填写化学式).
答案:略
解析:
提示:
解析:
|
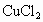 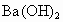
解析:根据题给信息, B为氯化物,C为碱,B、C溶液混合后出现的蓝色沉淀是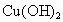 ,说明B中含 ,说明B中含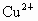 ,所以B为 ,所以B为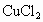 ,C为可溶性碱;A、C溶液混合后出现白色沉淀,该沉淀不溶于稀硝酸,说明该沉淀是AgCl或 ,C为可溶性碱;A、C溶液混合后出现白色沉淀,该沉淀不溶于稀硝酸,说明该沉淀是AgCl或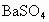 ,则C为AgOH或 ,则C为AgOH或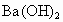 ,又因为AgOH不存在,所以C只能是 ,又因为AgOH不存在,所以C只能是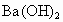 ,A、C混合产生的白色沉淀为 ,A、C混合产生的白色沉淀为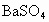 ,A是钠盐,所以A为 ,A是钠盐,所以A为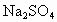 ;A、B混合,即 ;A、B混合,即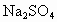 与 与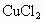 混合既无沉淀也无气体,不反应.所以A为 混合既无沉淀也无气体,不反应.所以A为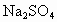 ,B为 ,B为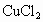 ,C为 ,C为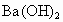 . . |
提示:
|
点拨:解此类题的关键是掌握酸、碱、盐之间的反应规律.以及常见典型沉淀的性质和常见酸、碱、盐的溶解性. |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目