题目内容
【题目】某小组的同学对实验室中一瓶放置已久的“生石灰”进行了如下的探究:
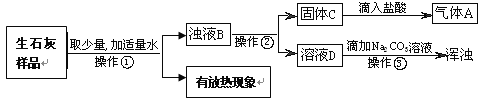
根据以上探究同学们对样品的组成提出了以下假设:
假设l.是Ca(OH)2和CaCO3的混合物,假设2.是CaO和CaCO3的混合物,
假设3.是_____的混合物.假设4.是Ca(OH)2和CaO的混合物
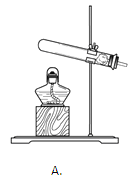
(1)图中操作②的名称是_____,玻璃棒的作用是_____
(2)通过实验现象可以直接看出,其中假设_____不合理.
(3)有同学认为此生石灰样品中一定有氢氧化钙,你认为他的说法_____(填正确或错误),因为_____;
为了得到最后结论,同学们继续进行实验:
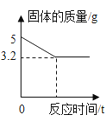
①称取0.75克样品,加足量的水充分溶解,过滤得滤液A和0.1克沉淀B;
②将滤液A等分成2份,一份先加少量酚酞试液再滴加稀盐酸至过量,得混合物C,另一份加过量的碳酸钠溶液,得混合物D;
③将混合物C、D倒入一个洁净的烧杯中,发现烧杯中有白色沉淀且上层清液呈红色,过滤,得滤液E和1g滤渣.
④向滤液E中滴加CaCl2溶液,有白色沉淀生成.
(4)则滤液E中一定含有的溶质是_____,可能含有_____,怎样验证滤液E中可能含有的物质一定存在_____
(5)根据实验现象及数据判断,原样品中一定含有的是_____
【答案】Ca(OH)2、CaCO3和CaO的混合物 过滤 引流 4 错误 氧化钙能和水反应生成氢氧化钙 氯化钠和碳酸钠 氢氧化钠 取少量滤液E于试管中,加入过量的氯化钙溶液,溶液仍显红色,证明一定有氢氧化钠 氧化钙、氢氧化钙、碳酸钙
【解析】
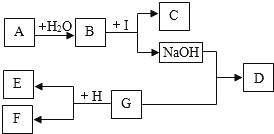
根据流程图步骤及现象可以得知,生石灰样品加适量水之后,有放热的现象,说明有氧化钙或氢氧化钙;得到浊液,进行操作②过滤之后得到固体C,往固体C中滴加盐酸有气泡产生,说明含有碳酸钙;往滤液D中滴加碳酸钠溶液,变浑浊,说明溶液中含有氢氧化钙。
根据流程图步骤及现象可以得知,生石灰样品加适量水之后,有放热的现象,说明有氧化钙或氢氧化钙;得到浊液,进行操作②过滤之后得到固体C,往固体C中滴加盐酸有气泡产生,说明含有碳酸钙;往滤液D中滴加碳酸钠溶液,变浑浊,说明溶液中含有氢氧化钙;
据此可以提出假设。假设l.是Ca(OH)2和CaCO3的混合物;假设2.是CaO和CaCO3的混合物;假设3.Ca(OH)2、CaCO3和CaO的混合物;假设4.是Ca(OH)2和CaO的混合物;故填:Ca(OH)2、CaCO3和CaO的混合物
(1)根据流程图操作分析,得操作②是固液分离,因此图中操作的名称是过滤,玻璃棒在过滤中的作用是引流;故填:过滤;引流
(2)通过实验现象,据分析生石灰样品中一定有碳酸钙,因此假设4不合理。故填:4
(3)因为氧化钙能和水反应生成氢氧化钙,只要加入了水,就不知道是否是原有的,还是由氧化钙与水反应产生的,因此认为此生石灰样品中一定有氢氧化钙,说法错误;故填:错误;氧化钙能和水反应生成氢氧化钙
为了得到最后结论,同学们继续进行实验:
①称取0.75克样品,加足量的水充分溶解,过滤得滤液A和0.1克碳酸钙沉淀B;说明原固体有碳酸钙;②将滤液A等分成2份,一份先加少量酚酞试液再滴加稀盐酸至过量,得混合物C,另一份加过量的碳酸钠溶液,得混合物D;③将混合物C、D倒入一个洁净的烧杯中,发现烧杯中有白色沉淀且上层清液呈红色,过滤,得滤液E和1g滤渣.④向滤液E中滴加CaCl2溶液,有白色沉淀生成.说明滤液E中有碳酸钠;
(4)根据以上实验可知,滤液E中一定含有的溶质是氯化钠和碳酸钠,可能含有氢氧化钠,为了验证滤液E中一定含有氢氧化钠,可以加入氯化钙把碳酸根除去,然后观察溶液颜色的变化,实验步骤可以是:取少量滤液E于试管中,加入过量的氯化钙溶液,除去碳酸根离子,若溶液仍显红色,证明一定有氢氧化钠;故填:氯化钠和碳酸钠;氢氧化钠;取少量滤液E于试管中,加入过量的氯化钙溶液,溶液仍显红色,证明一定有氢氧化钠
(5)根据实验现象及数据判断,原样品中一定含有的是氧化钙、氢氧化钙、碳酸钙;故填:氧化钙、氢氧化钙、碳酸钙

 优加精卷系列答案
优加精卷系列答案