题目内容
由Mg、Fe、CuO组成的混合物加入适量的盐酸,充分反应后铁有剩余,则该溶液中含有的金属阳离子是( )
分析:根据金属活动性顺序表及其应用分析.在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此回答问题即可;
解答:解:Mg、Fe、CuO三种物质分别于盐酸反应生成氯化镁、氯化亚铁和氯化铜的溶液;
A、由于铁的活动性比镁弱,所以铁不能置换出溶液中的镁离子(镁与盐酸的反应所得),故A正确;
B、铁的活动性比铜强,所以铁可以置换出氯化铜中的铜离子,由于充分反应后铁有剩余,所以溶液中一定不会含有铜离子,故B错误;
C、铁的活动性比铜强,所以铁可以置换出氯化铜中的铜离子,由于充分反应后铁有剩余,所以溶液中一定不会含有铜离子,故C错误;
D、铁的活动性比铜强,所以铁可以置换出氯化铜中的铜离子,由于充分反应后铁有剩余,所以溶液中一定不会含有铜离子,但会含有亚铁离子和镁离子,故D错误;
故选A
A、由于铁的活动性比镁弱,所以铁不能置换出溶液中的镁离子(镁与盐酸的反应所得),故A正确;
B、铁的活动性比铜强,所以铁可以置换出氯化铜中的铜离子,由于充分反应后铁有剩余,所以溶液中一定不会含有铜离子,故B错误;
C、铁的活动性比铜强,所以铁可以置换出氯化铜中的铜离子,由于充分反应后铁有剩余,所以溶液中一定不会含有铜离子,故C错误;
D、铁的活动性比铜强,所以铁可以置换出氯化铜中的铜离子,由于充分反应后铁有剩余,所以溶液中一定不会含有铜离子,但会含有亚铁离子和镁离子,故D错误;
故选A
点评:本题主要考查了对金属活动性顺序的灵活应用,只有活动性强的金属可以把活动性弱的金属从盐溶液中置换出来,培养学生分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
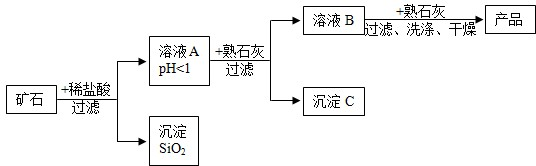
某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:
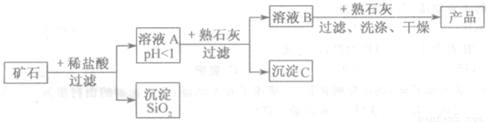
(1)溶液A中共含有 种阳离子;
(2)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的阳离子转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可允许的范围为 ;
|
氢氧化物 |
Fe(OH)3 |
Cu(OH)2 |
Mg(OH)2 |
|
开始沉淀的pH |
1.5 |
4.2 |
8.6 |
|
完全沉淀的pH |
3.2 |
6.7 |
11.1 |
(3)溶液B中一定含有的溶质为 (填化学式);
(4)写出溶液B中加入熟石灰,生成产品的化学方程式: 。
某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:
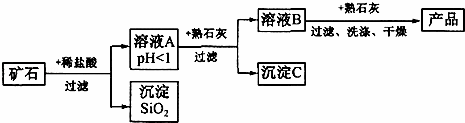
(1)溶液A中共含有 种阳离子;
(2)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀.该实验条件下,使金属阳离子沉淀的相关pH数据见下表.为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为 ;
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 8.6 |
| 完全沉淀的pH | 3.2 | 6.7 | 11.1 |
(3)溶液B中一定含有的溶质为 (填化学式);
(4)写出溶液B中加人熟石灰 ,生成产品的化学方程式: .
,生成产品的化学方程式: .