题目内容
在一烧杯中盛有稀H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央(如图所示)。向该烧杯里缓缓注入与稀H2SO4等密度的Ba(OH )2溶液至恰好完全反应。在此实验过程中
)2溶液至恰好完全反应。在此实验过程中
⑴烧杯里观察到的实验现象有:
①____________________________________________,
②____________________________________________。
⑵写出实验过程中反应的离子方程式
________________________________________。

⑴烧杯里观察到的实验现象有:①小球下沉②有白色沉淀
{2}2 H++SO42 -+Ba2++2OH-=2H2O+BaSO4↓

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
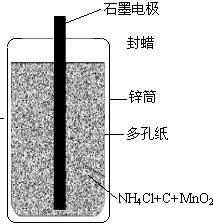 22、日常用的干电池构造、组成如图.某校化学活动小组正进行的研究性课题是
22、日常用的干电池构造、组成如图.某校化学活动小组正进行的研究性课题是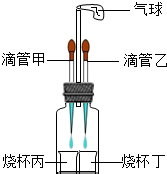 (2013?平顶山二模)如图所示装置(气密性良好),改变滴管和小烧杯中的物质可以完成多个简单实验.
(2013?平顶山二模)如图所示装置(气密性良好),改变滴管和小烧杯中的物质可以完成多个简单实验. 如图测所示,弹簧秤下挂着一重物A,烧杯中盛有溶液B,试根据要求回答下列问题:
如图测所示,弹簧秤下挂着一重物A,烧杯中盛有溶液B,试根据要求回答下列问题: