题目内容
【题目】海洋是巨大的资源宝库,人类正在运用各种方法开发、提取海洋资源。
(1)海水晒盐得粗盐,粗盐提纯的实验步骤为:溶解、过滤、蒸发结晶。三步操作中均用到的一种玻璃仪器是__________,蒸发操作中该仪器的作用是_______________。
(2)从海水中得到金属镁。用苦卤制取金属镁的流程图如图所示:
![]()
①步骤1发生反应的化学方程式为_____________。
②验证苦卤中MgCl2已完全转化为Mg(OH)2沉淀的方法是______________。
(3)海水制碱,流程图如图所示:
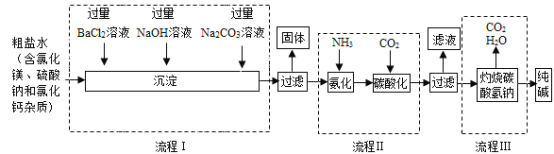
①该厂最终得到的产品有___________(填物质名称)。
②流程中加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,除掉的离子依次是_________(填离子符号,注意顺序)。
③写出流程Ⅱ中发生反应的化学方程式____________________。
【答案】玻璃棒 搅拌,防止由于局部温度过高,造成液滴飞溅 ![]() 取少量滤液于试管中,继续滴加氢氧化钙溶液,观察到没有沉淀生成 碳酸钠和氯化铵 SO42-、Mg2+、Ca2+、Ba2+
取少量滤液于试管中,继续滴加氢氧化钙溶液,观察到没有沉淀生成 碳酸钠和氯化铵 SO42-、Mg2+、Ca2+、Ba2+ ![]()
【解析】
(1)海水晒盐得粗盐,粗盐提纯的实验步骤为:溶解、过滤、蒸发结晶。三步操作中均用到的一种玻璃仪器是玻璃棒,蒸发操作中该仪器的作用是搅拌,防止局部温度过高,造成液滴飞溅;
(2)①步骤①为苦卤中的氯化镁和氢氧化钙反应,生成氢氧化镁和氯化钙,该反应的化学方程式为:![]() ;
;
②验证苦卤中MgCl2已完全转化为Mg(OH)2沉淀的方法是取少量滤液于试管中,继续滴加氢氧化钙溶液,观察到没有沉淀生成;
(3)①流程Ⅰ中产生的氯化钠可与NH3、CO2、H2O反应生成氯化铵和碳酸氢钠,在相同温度下,碳酸氢钠的溶解度较小,故碳酸氢钠先析出,碳酸氢钠可在加热的条件下,生成碳酸钠、二氧化碳和水,故该厂最终得到的产品有碳酸钠和氯化铵;
②氯化钡可与硫酸钠反应生成硫酸钡沉淀和氯化钠,其化学反应方程式为:![]() ,故氯化钡溶液除去的是SO42-;
,故氯化钡溶液除去的是SO42-;
氢氧化钠溶液可与氯化镁溶液反应生成氢氧化镁沉淀和氯化钠,其化学反应方程式为:![]() ,故氢氧化钠溶液除去的Mg2+;
,故氢氧化钠溶液除去的Mg2+;
碳酸钠可与氯化钙反应生成碳酸钙沉淀和氯化钠,其化学反应方程式为:![]() ,碳酸钠还能与氯化钡溶液形成碳酸钡沉淀和氯化钠,其化学反应方程式为:
,碳酸钠还能与氯化钡溶液形成碳酸钡沉淀和氯化钠,其化学反应方程式为:![]() 故碳酸钠除去的是Ca2+、Ba2+;
故碳酸钠除去的是Ca2+、Ba2+;
故除掉的离子依次是SO42-、Mg2+、Ca2+、Ba2+;
③流程Ⅱ中为氯化钠和氨气、二氧化碳、水生成氯化铵和碳酸氢钠,发生反应的化学方程式为:![]()