题目内容
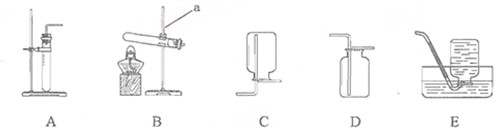
实验室制取常见气体所需装置如图1所示.请回答以下问题:
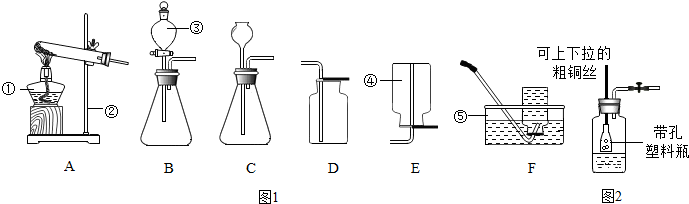
(1)写出如图1中带序号仪器的名称:
①
(2)选用发生装置
(3)实验室用加热高锰酸钾的方法制取氧气,应选用的发生装置是
(4)小红用家里的粗铜丝和废塑料药瓶组装成一套装置(如图2所示)用于完成制取某些气体的实验,这套装置得到了老师的表扬.
i.利用该装置做实验的优点是
①节约药品用量 ②能完全消除废液排放
③可控制反应的进程 ④产生的气体不含任何杂质
ii.该装置与如图1装置

(1)写出如图1中带序号仪器的名称:
①
酒精灯
酒精灯
; ②铁架台
铁架台
;③分液漏斗
分液漏斗
;④集气瓶
集气瓶
;⑤水槽
水槽
.(2)选用发生装置
B(或C)
B(或C)
(填标号,下同)可用来制取CO2,收集该气体可用装置D
D
,选用该收集装置的理由是二氧化碳的密度比空气大,易溶于水
二氧化碳的密度比空气大,易溶于水
,获得该种气体的反应文字表达式或化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
,验满方法是将一根燃着的木条放在集气瓶口,若木条熄灭,证明满了
将一根燃着的木条放在集气瓶口,若木条熄灭,证明满了
.(3)实验室用加热高锰酸钾的方法制取氧气,应选用的发生装置是
A
A
(填标号),反应的文字表达式或化学方程式为2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
. 用该装置制取氧气还应该在试管口
| ||
放一团棉花
放一团棉花
,目的是防止高锰酸钾进入导气管
防止高锰酸钾进入导气管
.(4)小红用家里的粗铜丝和废塑料药瓶组装成一套装置(如图2所示)用于完成制取某些气体的实验,这套装置得到了老师的表扬.
i.利用该装置做实验的优点是
①③
①③
(填序号).①节约药品用量 ②能完全消除废液排放
③可控制反应的进程 ④产生的气体不含任何杂质
ii.该装置与如图1装置
B
B
(选填“B”或“C”)在制取气体时具有相类似的优点.分析:(1)熟练掌握常见的化学仪器及其用途;
(2)根据反应物的状态和反应条件选择发生装置;根据气体密度和溶解性选择收集方法;验满二氧化碳的方法是:将一根燃着的木条放在集气瓶口,看木条是否熄灭;
(3)根据反应物的状态和反应条件选择发生装置;根据实验的注意事项回答;
(4)根据装置的特点分析选择装置的优点.
(2)根据反应物的状态和反应条件选择发生装置;根据气体密度和溶解性选择收集方法;验满二氧化碳的方法是:将一根燃着的木条放在集气瓶口,看木条是否熄灭;
(3)根据反应物的状态和反应条件选择发生装置;根据实验的注意事项回答;
(4)根据装置的特点分析选择装置的优点.
解答:解:(1)①是酒精灯;②是铁架台;③是分液漏斗;④是集气瓶;⑤是水槽;
(2)在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,故发生装置的特点属于固液常温型的B(或C)装置;
根据二氧化碳的密度比空气大,易溶于水的特点选择的收集方法是向上排空气法的D装置;反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
验满二氧化碳的方法是:将一根燃着的木条放在集气瓶口,若木条熄灭,证明满了;
(3)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,故发生装置的特点属于固体加热型的A装置;
反应的方程式为:2KMnO4
K2MnO4+MnO2+O2↑;
用高锰酸钾制取氧气时要在试管口放一团棉花;其作用是防止高锰酸钾颗粒随着气流带入导管;
(4)用粗铜丝和废塑料药瓶组装成的装置可以通过上下移动的粗铜丝控制反应的发生和停止,因此装置的优点是:节约药品用量;可控制反应的进程;但不能完全消除废液排放
;产生的气体可能含有杂质;该装置类似与装置B,分液漏斗可以控制反应速率.
故答案为:(1)酒精灯;铁架台;分液漏斗;集气瓶;水槽;
(2)B(或C);D;二氧化碳的密度比空气大,易溶于水;CaCO3+2HCl=CaCl2+H2O+CO2↑;将一根燃着的木条放在集气瓶口,若木条熄灭,证明满了;
(3)A;2KMnO4
K2MnO4+MnO2+O2↑;放一团棉花;防止高锰酸钾进入导气管;
(4)①③;B.
(2)在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,故发生装置的特点属于固液常温型的B(或C)装置;
根据二氧化碳的密度比空气大,易溶于水的特点选择的收集方法是向上排空气法的D装置;反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
验满二氧化碳的方法是:将一根燃着的木条放在集气瓶口,若木条熄灭,证明满了;
(3)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,故发生装置的特点属于固体加热型的A装置;
反应的方程式为:2KMnO4
| ||
用高锰酸钾制取氧气时要在试管口放一团棉花;其作用是防止高锰酸钾颗粒随着气流带入导管;
(4)用粗铜丝和废塑料药瓶组装成的装置可以通过上下移动的粗铜丝控制反应的发生和停止,因此装置的优点是:节约药品用量;可控制反应的进程;但不能完全消除废液排放
;产生的气体可能含有杂质;该装置类似与装置B,分液漏斗可以控制反应速率.
故答案为:(1)酒精灯;铁架台;分液漏斗;集气瓶;水槽;
(2)B(或C);D;二氧化碳的密度比空气大,易溶于水;CaCO3+2HCl=CaCl2+H2O+CO2↑;将一根燃着的木条放在集气瓶口,若木条熄灭,证明满了;
(3)A;2KMnO4
| ||
(4)①③;B.
点评:本题考查了常见气体的制取和收集及实验的注意事项;关键是掌握其选择的依据及原理,在装置的分析中明确装置的特点及其作用,难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目