题目内容
今年冬天天气比较寒冷,市场上各种各样的保暖袋热销.(1)有一种发热产品“热宝”暖手袋(密封性好)很有特色,初次使用只要用手揉搓袋内的液体,一段时间后,温度就会升高;当停止揉搓,冷却到室温时,袋内的液体中会有固体物质;再次使用时,只要把“热宝”放入沸水中加热,使袋内固体消失后,再次用手揉搓袋内的液体,温度便又会升高.因此,此产品可反复使用达千次以上.
查阅资料:袋内的液体是醋酸钠的“过饱和溶液”.
Ⅰ.在一定温度和压力的条件下,当溶液中溶质的质量分数已超过该温度和压力下饱和溶液的溶质质量分数,而溶质仍不析出的现象叫过饱和现象,此时的溶液称为过饱和溶液.
Ⅱ.醋酸钠“过饱和溶液”的配制方法:室温下,先向装有醋酸钠饱和溶液的烧杯中加入一定量的醋酸钠晶体,再将烧杯放在到电热板上加热,使晶体完全溶解,最后将该溶液急速冷却到室温(冷却过程中无晶体析出).
Ⅲ.醋酸钠“过饱和溶液”是一种处于不稳定状态的溶液,其不稳定性主要体现在:若溶液受到振动或者向溶液中加入溶质晶体,溶液中便会出现晶核--溶质析出的聚集中心,这时溶液中过量溶解的溶质就会析出而成为饱和溶液,即转化为稳定状态.
分析问题:根据上述材料,回答如下问题:
①醋酸钠固体的溶解度随温度的升高而______(选填“不变”、“增大”或“减小”).
②在使用过程中,“热宝”暖手袋内液体中产生的固体物质是______.
③醋酸钠的“过饱和溶液”转变成饱和溶液的过程是一个______(填“吸热”或“放热”)过程.
④实验室的桌面上现有一个装有醋酸钠“过饱和溶液”的烧杯,若要使溶质从溶液中析出,可采取下列方法中的______
a.加入少量醋酸钠晶体 b.摩擦烧杯壁,产生玻璃碎末 c.过度冷却 d.用玻璃棒搅拌
A.a B.a、b C.a、b、d D.a、b、c、d
(2)某沿海地区的食品厂开发生产了一种保暖袋深受中小学生喜爱.剪开保暖袋的外层塑料,会发现袋内有一小袋红色液体和一些固态物.红色液体是一种溶解了有香味的色素的水溶液.
使用时,用手拍打几下保暖袋,让袋内红色液体与固态物接触,3至5分钟保暖袋的温度就达70度以上.
提出问题:袋内的固态物是什么?
进行猜想:猜想1:固态物是氢氧化钠;猜想2:固态物是A物质;猜想3:固态物是硝酸铵.
上述猜想中,猜想3肯定不成立的理由是______.
实验验证:为了验证其他两种猜想,某化学兴趣小组开展了如下探究:
Ⅰ.查阅资料发现,氢氧化钠的主要性质:①一种易溶于水的白色固体;②能够使无色酚酞变红色;③能和二氧化碳气体反应,反应的化学方程式:2NaOH+CO2=Na2CO3+H2O,且反应生成的Na2CO3易溶于水.
Ⅱ.请完成如下探究实验表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 取袋内固体与一定量的水混合后于烧杯中,充分搅拌后过滤,向滤液中______. | ______ | 猜想2正确 |
【答案】分析:(1)Ⅲ.①根据题中信息判断;
②根据醋酸钠溶液揉搓产生固体分析;
③根据“热宝”暖手袋的作用分析;
④a.根据醋酸钠“过饱和溶液”中加入少量醋酸钠晶不会再溶解分析;
b.根据热宝”暖手袋的使用方法可知摩擦烧装有醋酸钠“过饱和溶液”的烧杯会产生晶体分析;
c.根据将醋酸钠过饱和溶液急速冷却到室温,冷却过程中无晶体析出分析;
d.根据饱和的醋酸钠溶液振动便会产生晶体分析;
(2)进行猜想:根据硝酸铵形成溶液温度会降低分析;
Ⅱ.根据氢氧化钠有腐蚀性,硝酸铵已排除,所以保暖袋内的物质是A物质,即是氧化钙;
反思评价:①氧化钙的化学式为:CaO;高温煅烧石灰水可得生石灰;
②根据在水中加入一些杂质能改变水的凝固点分析;
③保暖袋在使用上与装有醋酸钠“过饱和溶液”的热宝相比教进行分析;
解答:解:(1)Ⅲ.①将醋酸钠晶体放在到电热板上加热使晶体完全溶解,可知醋酸钠固体的溶解度随温度的升高而增大,故填:增大;
②由题意知,醋酸钠溶液揉搓产生固体,所以固体是析出的醋酸钠晶体,故填:醋酸钠晶体;
③由“热宝”暖手袋的作用可知醋酸钠的“过饱和溶液”转变成饱和溶液的过程是一个放热过程,故填:放热;
④a.在醋酸钠“过饱和溶液”中加入少量醋酸钠晶不会再溶解,所以有晶体存在,故a正确;
b.由热宝”暖手袋的使用方法可知摩擦烧装有醋酸钠“过饱和溶液”的烧杯会产生晶体,故b正确;
c.将醋酸钠过饱和溶液急速冷却到室温,冷却过程中无晶体析出,所以过度冷却醋酸钠过饱和溶液不会析出晶体,故c错误;
d.由题意知,饱和的醋酸钠溶液振动便会产生晶体,所以搅拌也会产生晶体,故d正确;
(2)进行猜想:硝酸铵形成溶液温度会降低,所以保暖袋内不会放有硝酸铵,故填:硝酸铵形成溶液温度会降低;
Ⅱ.氢氧化钠有腐蚀性,所以保暖袋内的物质不可能是,硝酸铵已排除,所以保暖袋内的物质是A物质,即可推测是氧化钙,所以取袋内物质溶于水,形成氢氧化钙溶液,通入二氧化碳,溶液变浑浊,故填:通入二氧化碳;溶液变浑浊;
反思评价:①氧化钙的化学式为:CaO;高温煅烧石灰水可得生石灰,反应的化学方程式为:CaCO3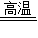 CaO+CO2↑;因为氧化钙能与水反应,所以氧化钙可以作干燥剂;故填:CaO;CaCO3
CaO+CO2↑;因为氧化钙能与水反应,所以氧化钙可以作干燥剂;故填:CaO;CaCO3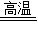 CaO+CO2↑;干燥剂;
CaO+CO2↑;干燥剂;
②在水中加入一些杂质能改变水的凝固点,所以向水中添加一些易溶性色素能降低水的凝固点,故填:降低水的凝固点;
③保暖袋在使用上与装有醋酸钠“过饱和溶液”的热宝相比,一个明显的优点是使用方便,故填:使用方便;
点评:本题通过日常生活中的用品考查了所学的化学知识,真正体现了学有所用.
②根据醋酸钠溶液揉搓产生固体分析;
③根据“热宝”暖手袋的作用分析;
④a.根据醋酸钠“过饱和溶液”中加入少量醋酸钠晶不会再溶解分析;
b.根据热宝”暖手袋的使用方法可知摩擦烧装有醋酸钠“过饱和溶液”的烧杯会产生晶体分析;
c.根据将醋酸钠过饱和溶液急速冷却到室温,冷却过程中无晶体析出分析;
d.根据饱和的醋酸钠溶液振动便会产生晶体分析;
(2)进行猜想:根据硝酸铵形成溶液温度会降低分析;
Ⅱ.根据氢氧化钠有腐蚀性,硝酸铵已排除,所以保暖袋内的物质是A物质,即是氧化钙;
反思评价:①氧化钙的化学式为:CaO;高温煅烧石灰水可得生石灰;
②根据在水中加入一些杂质能改变水的凝固点分析;
③保暖袋在使用上与装有醋酸钠“过饱和溶液”的热宝相比教进行分析;
解答:解:(1)Ⅲ.①将醋酸钠晶体放在到电热板上加热使晶体完全溶解,可知醋酸钠固体的溶解度随温度的升高而增大,故填:增大;
②由题意知,醋酸钠溶液揉搓产生固体,所以固体是析出的醋酸钠晶体,故填:醋酸钠晶体;
③由“热宝”暖手袋的作用可知醋酸钠的“过饱和溶液”转变成饱和溶液的过程是一个放热过程,故填:放热;
④a.在醋酸钠“过饱和溶液”中加入少量醋酸钠晶不会再溶解,所以有晶体存在,故a正确;
b.由热宝”暖手袋的使用方法可知摩擦烧装有醋酸钠“过饱和溶液”的烧杯会产生晶体,故b正确;
c.将醋酸钠过饱和溶液急速冷却到室温,冷却过程中无晶体析出,所以过度冷却醋酸钠过饱和溶液不会析出晶体,故c错误;
d.由题意知,饱和的醋酸钠溶液振动便会产生晶体,所以搅拌也会产生晶体,故d正确;
(2)进行猜想:硝酸铵形成溶液温度会降低,所以保暖袋内不会放有硝酸铵,故填:硝酸铵形成溶液温度会降低;
Ⅱ.氢氧化钠有腐蚀性,所以保暖袋内的物质不可能是,硝酸铵已排除,所以保暖袋内的物质是A物质,即可推测是氧化钙,所以取袋内物质溶于水,形成氢氧化钙溶液,通入二氧化碳,溶液变浑浊,故填:通入二氧化碳;溶液变浑浊;
反思评价:①氧化钙的化学式为:CaO;高温煅烧石灰水可得生石灰,反应的化学方程式为:CaCO3
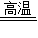 CaO+CO2↑;因为氧化钙能与水反应,所以氧化钙可以作干燥剂;故填:CaO;CaCO3
CaO+CO2↑;因为氧化钙能与水反应,所以氧化钙可以作干燥剂;故填:CaO;CaCO3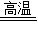 CaO+CO2↑;干燥剂;
CaO+CO2↑;干燥剂;②在水中加入一些杂质能改变水的凝固点,所以向水中添加一些易溶性色素能降低水的凝固点,故填:降低水的凝固点;
③保暖袋在使用上与装有醋酸钠“过饱和溶液”的热宝相比,一个明显的优点是使用方便,故填:使用方便;
点评:本题通过日常生活中的用品考查了所学的化学知识,真正体现了学有所用.

练习册系列答案
相关题目