题目内容
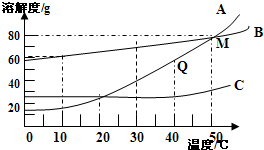 如图是A、B、C三种物质的溶解度曲线.据图,回答下列问题.
如图是A、B、C三种物质的溶解度曲线.据图,回答下列问题.
(1)30℃时,三种物质溶解度从大到小顺序为______.
(2)M点的意义是______.
(3)如果A中混有少量的C,可以采取______方法提纯A.
(4)现有50℃的A、C两份饱和溶液,要使溶液的溶质质量分数相同,且溶液仍是饱和的,采取的方法是______.
解:(1)30℃时,三种物质溶解度从大到小顺序为:B>A>C;
(2)M点是50℃时AB两种物质溶解度的曲线的交点,表示该温度下两物质的溶解度相等;
(3)由图可知:A 的溶解度受温度影响较大,C的溶解度受温度影响较小,所以如果A中混有少量的C,可以采取 蒸发结晶的方法提纯A;
(4)由图可知:AC的溶解度均随温度的升高而降低,且20℃时二者的溶解度相等,则其饱和溶液的溶质质量分数在该温度下也相等,所以50℃的A、C两份饱和溶液,要使溶液的溶质质量分数相同,且溶液仍是饱和的,可将温度降温至20℃;
故答案为:(1)B>A>C;
(2)在50℃时,AB两种物质的溶解度相同为50g;
(3)蒸发结晶;
(4)降温至20℃.
分析:(1)根据A、B、C、三种固体物质的溶解度曲线,比较在t1℃时,A、B、C三种物质的溶解度的大小;
(2)根据溶解度曲线交点的意义分析;
(3)根据AC的溶解度随温度变化情况分析提纯A的方法;
(4)根据饱和时质量分数的计算式 ×100%,即溶解度相等则质量分数也就相等.
×100%,即溶解度相等则质量分数也就相等.
点评:本题主要考查了溶解度曲线的意义、饱和溶液中溶质的质量分数计算等知识,掌握相关知识才能顺利解答.
(2)M点是50℃时AB两种物质溶解度的曲线的交点,表示该温度下两物质的溶解度相等;
(3)由图可知:A 的溶解度受温度影响较大,C的溶解度受温度影响较小,所以如果A中混有少量的C,可以采取 蒸发结晶的方法提纯A;
(4)由图可知:AC的溶解度均随温度的升高而降低,且20℃时二者的溶解度相等,则其饱和溶液的溶质质量分数在该温度下也相等,所以50℃的A、C两份饱和溶液,要使溶液的溶质质量分数相同,且溶液仍是饱和的,可将温度降温至20℃;
故答案为:(1)B>A>C;
(2)在50℃时,AB两种物质的溶解度相同为50g;
(3)蒸发结晶;
(4)降温至20℃.
分析:(1)根据A、B、C、三种固体物质的溶解度曲线,比较在t1℃时,A、B、C三种物质的溶解度的大小;
(2)根据溶解度曲线交点的意义分析;
(3)根据AC的溶解度随温度变化情况分析提纯A的方法;
(4)根据饱和时质量分数的计算式
 ×100%,即溶解度相等则质量分数也就相等.
×100%,即溶解度相等则质量分数也就相等.点评:本题主要考查了溶解度曲线的意义、饱和溶液中溶质的质量分数计算等知识,掌握相关知识才能顺利解答.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
 17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题.
17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题. 29、如图是a、b、c三种固体物质的溶解度曲线图.
29、如图是a、b、c三种固体物质的溶解度曲线图. 16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答:
16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答: (1)如图是A、B、C三种物质的溶解度曲线.请回答:
(1)如图是A、B、C三种物质的溶解度曲线.请回答:
