题目内容
【题目】I.已知A、B、C、D、E五种物质中均含有某种相同的非金属元素,B为无色液体,C为黑色固体,D气体能使澄清石灰水变浑浊。图中“→”表示物质之间的转化关系。五种物质的转化关系如图所示(图中反应条件及部分反应物或生成物省略)。

(1)A、E的化学式分别是_____________、__________________。
(2)A→C反应的化学方程式是___________________________。
(3)A→B反应的化学方程式是___________________________。
II.工业制取硝酸的流程如下:
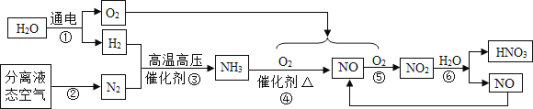
(1)步骤②是利用了氮气与氧气____________的不同,是____________变化(填“物理“或”化学“)。
(2)步骤③是化合反应,写出③的化学方程式为_______________________________。
(3)步骤④的化学方程式为 4NH3+5O2![]() 4NO+6X,X的化学式为_________________。
4NO+6X,X的化学式为_________________。
(4)流程中一定要循环使用的物质是_____________________(写化学式)。
【答案】O2 CaCO3 3Fe+2O2![]() Fe3O4 2H2+O2
Fe3O4 2H2+O2![]() 2H2O 沸点 物理 N2+3H2
2H2O 沸点 物理 N2+3H2![]() 2NH3 H2O NO
2NH3 H2O NO
【解析】
I.B为无色液体,可以和A相互转化,A可以转化为C,C是黑色固体,因此B可以是水,则A是氧气,C是四氧化三铁;D气体能使澄清石灰水变浑浊,故D是二氧化碳,A、B、C、D、E五种物质中均含有某种相同的非金属元素,因此相同的元素是氧元素;结合转化关系,E可以是碳酸钙,碳酸钙和盐酸反应产生氯化钙、水和二氧化碳,二氧化碳和氢氧化钙反应产生碳酸钙沉淀和水,带入题干,推断合理。
I. 由分析可知(1)A是氧气,E是碳酸钙,化学式分别为:O2,CaCO3;
(2)A→C是氧气和铁点燃生成四氧化三铁,反应的化学方程式:3Fe+2O2![]() Fe3O4;
Fe3O4;
(3)A→B是氧气和氢气点燃生成水,反应的化学方程式:2H2+O2![]() 2H2O;
2H2O;
II.(1)分离液态空气原理是利用氮气和氧气的沸点不同,先将空气加压变成液态,然后再加热,由于氮气的沸点比氧气的低,氮气先从液态空气中蒸发出来,留下的就是氧气;蒸发是物质的三态变化之一,是物理变化;
(2)步骤③是化合反应,是氢气和氮气在高温高压加催化剂条件下生成氨气,反应方程式为:N2+3H2![]() 2NH3;
2NH3;
(3)根据化学反应前后元素种类不变,原子的个数不变以及化学方程式 4NH3+5O2![]() 4NO+6X分析,解得X 中含有H、O元素,个数分别为12和6,又X前面系数为6,所以X的化学式H2O;
4NO+6X分析,解得X 中含有H、O元素,个数分别为12和6,又X前面系数为6,所以X的化学式H2O;
(4)既是反应物,也是生成物的物质可以循环使用,所以流程中一定要循环使用的物质是NO。

 同步轻松练习系列答案
同步轻松练习系列答案【题目】早在十七世纪,英国化学家波义耳由于实验设计“失误”,错过了发现质量守恒定律的机会,请你改进他的试验方法,以验证质量守恒定律。
波义耳的实验(1673年) | 我的改进 |
在密闭的容器中燃烧金属,得到了金属灰 | 称量密闭的容器(连同里面的金属),进行燃烧实验 |
打开容器,称量金属灰的质量 | 燃烧结束后,称量________________ |
发现比原金属质量_____________(填“增加”或“减少”或“不变”) | 发现总质量和燃烧前一样。若反应容器内的反应是镁带燃烧,其反应的化学方程式是 _____________________________________ |
启发:用实验来研究化学反应前后反应物和生成物之间的质量关系时,应该在______________ 容器中进行。 | |
拓展:应用质量守恒定律验证石墨的元素组成。 实验步骤:称量a克石墨,放在盛有足量氧气的密闭容器中引燃;反应结束后,用足量的b克澄清石灰水吸收生成的气体(吸收完全),发生的反应方程式为:____________________ 称量石灰水的质量变为c克。 根据______________________________(现象),可知石墨中含有碳元素; 根据a=_______________________(用含b、c的关系式表示),可知石墨中只含有碳元素 | |
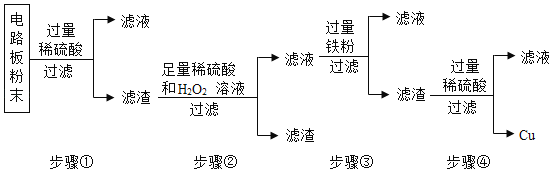
【题目】某矿石由MgO、Fe2O3、CuO、SiO2组成,先将矿石粉碎,再用它制备氢氧化镁,流程示意图如图所示:
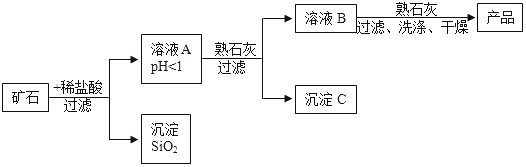
(1)矿石粉碎的目的是___________。
(2)溶液A中共含有________种阳离子。
(3)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。
氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀的pH | 1.5 | 4.2 | 8.6 |
完全沉淀的pH | 3.2 | 6.7 | 11.1 |
为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为__________,溶液B中一定含有的溶质为_______。