题目内容
【题目】2020年1月25日总建筑面积为3.39万平方米的火神山医院正式开工,火神山医院在建造过程中用到了HDPE膜。老师告诉同学们HDPE膜具有极好的抗冲击性和防潮性,听完老师的描述后,同学们对HDPE膜的组成元素产生了浓厚的兴趣,进行了如下探究。
(提出问题)HDPE膜由什么元素组成?
(查阅资料)①HDPE膜能够燃烧,燃烧可能生成一氧化碳;②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
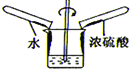
(实验探究)如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D(装置中每步反应均进行完全)。
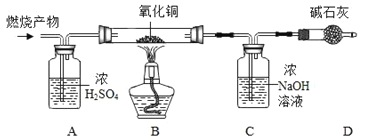
(实验记录)
装置质量 | A装置总质量 | C装置总质量 |
实验前 | 100.0g | 100.0g |
实验后 | 105.4g | 113.2g |
(实验分析)
(1)实验前,先通入氮气的目的是________。
(2)装置A中浓硫酸的作用是吸收_____________。
(3)实验中观察到装置B中黑色粉末变成红色,证明燃烧产物中有____________。
(4)装置C中发生的化学反应方程式为____________。
(5)装置D的作用是________________。
(数据处理)4.2g的HDPE膜样品中含碳元素的质量为____________g,含氢元素的质量为________g。
(实验结论)HDPE膜由碳元素、氢元素组成,不含其他元素的理由是生成物中碳、氢元素质量之和为_________(用数据分析)。
(反思拓展)实验中的4.2gHDPE膜样品燃烧消耗的氧气质量为m,则m的取值范围为______。
【答案】排尽装置内的空气,以防止燃烧可能生成一氧化碳时,加热发生爆炸 吸收水蒸气 一氧化碳 2NaOH+CO2═Na2CO3+H2O 防止外界空气中的水、二氧化碳等气体进入C装置,影响测量结果 3.6 0.6 生成物中碳、氢元素质量之和为4.2g 9.6g≤m<14.4g
【解析】
实验
(1)实验前,先通入氮气的目的是排尽装置内的空气,因为HDPE膜燃烧可能产生一氧化碳,一氧化碳具有可燃性,混有一定量的空气,遇明火容易爆炸,故填:排尽装置内的空气,以防止燃烧可能生成一氧化碳时,加热发生爆炸。
(2)浓硫酸具有吸水性,可以吸收水蒸气,故装置A中浓硫酸的作用是吸收水蒸气。故填:吸收水蒸气;
(3)实验中观察到装置B中黑色粉末变成红色,是因为氧化铜和一氧化碳在加热的条件下反应生成了铜,证明燃烧产物中有一氧化碳。故填:一氧化碳。
(4)装置C中氢氧化钠和二氧化碳反应生成碳酸钠和水,发生的化学反应方程式为:![]() ,故填:
,故填:![]() ;
;
(5)碱石灰能吸收空气中的水和二氧化碳,防止外界空气中的水、二氧化碳等气体进入C装置,影响测量结果。故填:防止外界空气中的水、二氧化碳等气体进入C装置,影响测量结果;
数据处理:
A装置增加的质量为HDPE膜燃烧生成水的质量,故生成水的质量为:105.4g-100.0g=5.4g;
C装置增加的质量为HDPE膜燃烧生成二氧化碳的质量和氧化铜与一氧化碳反应生成二氧化碳的质量之和,由![]() 可知,一氧化碳中的碳全部转化到了生成的二氧化碳中,故HDPE膜中的碳全部转化到了二氧化碳中,生成二氧化碳的总质量为:113.2g-100.0g=13.2g,
可知,一氧化碳中的碳全部转化到了生成的二氧化碳中,故HDPE膜中的碳全部转化到了二氧化碳中,生成二氧化碳的总质量为:113.2g-100.0g=13.2g,
4.2gHDPE膜样品中含碳元素的质量为:![]() ;
;
4.2gHDPE膜样品中含氢元素的质量为:![]()
实验结论:
HDPE膜由碳元素、氢元素组成,不含其他元素的理由:生成物中碳、氢元素质量之和为3.6g+0.6g=4.2g。
故填:生成物中碳、氢元素质量之和为4.2g。
反思拓展:
根据质量守恒定律,化学反应前后,元素的质量不变,故HDPE膜完全燃烧生成二氧化碳和水,消耗氧气的质量即生成的二氧化碳和水中氧元素的质量之和,生成二氧化碳中碳元素的质量与HDPE膜中碳元素质量相同,设生成的二氧化碳中氧元素质量为a,![]() ,a=9.6g,生成的水中氧元素的质量为:
,a=9.6g,生成的水中氧元素的质量为:![]()
故完全燃烧消耗氧气的质量为:9.6g+4.8g=14.4g
不完全燃烧全部生成一氧化碳和水时,消耗氧气质量,即生成的一氧化碳中氧元素的质量与生成的水中氧元素质量之和,设生成的一氧化碳中氧元素质量为b,![]() ,b=4.8g,
,b=4.8g,
故不完全燃烧消耗氧气的质量为:4.8g+4.8g=9.6g;
由于反应生成了一氧化碳,因此生成的气体可能全部是一氧化碳,也可能是一氧化碳和二氧化碳,则m的取值范围为:9.6g≤m<14.4g。
故填:9.6g≤m<14.4g。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案