题目内容
【题目】在一定温度下,向20gNa2CO3和NaCl的固体混合物中加入101g水,溶解后,再向其中加入100gCaCl2溶液恰好完全反应,过滤,所得滤液的质量为211g,将滤渣洗涤、干燥,称其质量为m,试计算: 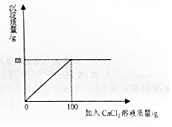
(1)m=g.
(2)当恰好完全反应时,所得溶液中溶质的质量分数为多少?
【答案】
(1)10
(2)解:设碳酸钠质量为x,反应生成氯化钠质量为y,
Na2CO3+CaCl2═ | CaCO3↓+ | 2NaCl |
106 | 100 | 117 |
x | 10g | y |
![]() =
= ![]() =
= ![]() ,
,
x=10.6g,y=11.7g,
当恰好完全反应时,所得溶液中溶质的质量分数为: ![]() ×100%=10%,
×100%=10%,
答:当恰好完全反应时,所得溶液中溶质的质量分数为10%
【解析】解:(1)m=20g+101g+100g﹣211g=10g. 故填:10.
【考点精析】解答此题的关键在于理解根据化学反应方程式的计算的相关知识,掌握各物质间质量比=系数×相对分子质量之比.

练习册系列答案
相关题目