题目内容
【题目】将某些化学知识用图式表示,既简明又扼要.以下Ⅰ和Ⅱ为两种常见的图式: 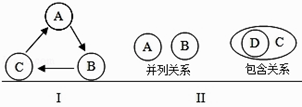
(1)物质的转化关系可用图式Ⅰ表示,“→”表示反应一步完成转化.若A、B、C分别为CaCO3 , CaO,Ca(OH)2 , 则A→B是反应(填反应类型),B→C的化学方程式是;若A为CaCO3 , C为Na2CO3 , 则B的是(填化学式).
(2)化学概念在逻辑上存在并列、包含和交叉关系.图式Ⅱ中,A与B是并列关系,如酸与碱;C与D是包含关系,如单质与非金属.若用A,B,C分别代表置换反应、复分解反应、中和反应,仿照图式Ⅱ的表示方法,将它们三者关系表示出来(A,B,C不要重复) .
【答案】
(1)分解;CaO+H2O═Ca(OH)2;CO2
(2)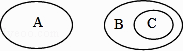
【解析】解:(1)若A、B、C分别为CaCO3 , CaO,Ca(OH)2 , 则碳酸钙转变成氧化钙要通过高温煅烧,发生的分解反应;CaO→Ca(OH)2 的方法是氧化钙和水发生化合反应,化学方程式是 CaO+H2O═Ca(OH)2;若A为CaCO3 , C为Na2CO3 , 则B的是一种能由碳酸钙反应生成,且能通过反应生成碳酸钠的物质,通过分析二氧化碳题意;所以答案是:分解; CaO+H2O═Ca(OH)2 , CO2 . (2)置换反应和复分解反应都属于化学基本反应类型,属于并列关系,中和反应是一类特殊的复分解反应,它们属于包含关系;所以答案是: 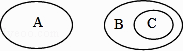
【考点精析】认真审题,首先需要了解中和反应及其应用(中和反应:酸与碱作用生成盐和水的反应),还要掌握置换反应及其应用(置换反应:一种单质和一种化合物反应,生成另一种单质和另一种化合物的反应)的相关知识才是答题的关键.

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】实验室中有一瓶久置的氢氧化钠溶液,以下实验设计合理的是( )
序号 | 实验目的 | 实验操作 |
① | 证明溶液发生变质 | 取少量溶液,加入足量稀盐酸 |
② | 确定溶液中溶质的成分 | 取少量溶液,加入适量氢氧化钡溶液,过滤,向滤液中滴加酚酞溶液 |
③ | 测定溶液中碳酸钠的质量分数 | 取一定质量溶液,加入足量稀盐酸,将生成的气体通入浓硫酸,测浓硫酸的增重 |
④ | 除去溶液中的碳酸钠 | 向溶液中滴加氢氧化钡溶液至恰好完全反应,过滤 |
A.①②
B.②③
C.①④
D.②④
【题目】小黄同学为了测定某混合物(Na2CO3与NaOH混合)中碳酸钠的质量分数,进行了如下实验:称取了20g样品配成溶液,然后逐渐加入一定量质量分数为20.8%的BaCl2溶液(已知:Na2CO3+BaCl2=2NaCl+BaCO3↓),充分反应.在此过程中他进行了三次数据测定,结果如下表:
测定次数 | 第1次 | 第2次 | 第3次 |
加入BaCl2溶液的质量/g | 60 | 120 | 150 |
生成沉淀的质量/g | 11.82 | 19.7 | 19.7 |
请分析数据,回答下列问题:
(1)第一次测定数据后所得溶液中含有溶质是NaOH,(填化学式);
(2)此实验中,实际参加反应的BaCl2溶液的质量为;
(3)样品中碳酸钠的质量分数为多少?(写出计算过程)
