题目内容
【题目】如图所示课本实验现象和结论都正确的是( )
A.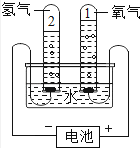
产生氢气和氧气的质量比为2:1,证明水是由氢氧元素组成
B.
量筒中水的质量越来越少,说明分子间存在间隔
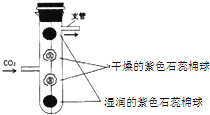
C.
蜡烛逐渐熄灭,说明物质燃烧需要达到可燃物的着火点
D.
铝丝表面出现红色物质,说明铝的金属活动性比铜强
【答案】D
【解析】解:A、电解水产生了氢气和氧气,根据质量守恒定律可以判断水是由氢氧两种元素组成的,电解水产生的氢气和氧气的体积比为2:1,故选项错误;
B、蒸发现象会使液体减少,故选项错误;
C、盐酸和碳酸钠反应产生二氧化碳,使蜡烛与氧气隔绝,熄灭,故选项错误;
D、铝丝表面出现红色物质,是铝把硫酸铜中的铜置换出来,说明铝的金属活动性比铜强,故选项正确;
故选项为:D.
【考点精析】通过灵活运用电解水实验和金属活动性顺序及其应用,掌握电解水的实验:A.装置―――水电解器B.电源种类---直流电C.加入硫酸或氢氧化钠的目的----增强水的导电性D.化学反应:2H2O=== 2H2↑+ O2↑;在金属活动性顺序里:1、金属的位置越靠前,它的活动性就越强2、位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸)3、位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来.(除K、Ca、Na)即可以解答此题.

练习册系列答案
相关题目