题目内容
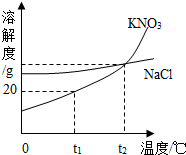 (2013?南京二模)如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
(2013?南京二模)如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )分析:A、比较物质的溶解度大小,须确定温度;
B、据饱和溶液中溶质的质量分数计算式分析解答;
C、不知溶液的质量,无法比较饱和溶液中溶质的质量关系;
D、一定温度下的饱和溶液中物质的溶解度相等,则溶质的质量分数相等.
B、据饱和溶液中溶质的质量分数计算式分析解答;
C、不知溶液的质量,无法比较饱和溶液中溶质的质量关系;
D、一定温度下的饱和溶液中物质的溶解度相等,则溶质的质量分数相等.
解答:解:A、不知温度,无法比较NaCl的溶解度大于KNO3的溶解度大小,故错误;
B、t1℃时,KNO3的溶解度是20g,所以其饱和溶液中溶质的质量分数是
×100%<20%,正确;
C、不知溶液的质量,无法比较饱和溶液中溶质的质量关系,故错误;
D、t2℃时的NaCl溶液与KNO3溶液中,溶质的质量分数不一定相等,若为饱和溶液,则该温度下其溶解度相等、溶质的质量分数也相等,现在溶液状态不确定,所以溶质的质量分数无法比较,故错误;
故选B.
B、t1℃时,KNO3的溶解度是20g,所以其饱和溶液中溶质的质量分数是
| 20g |
| 100g+20g |
C、不知溶液的质量,无法比较饱和溶液中溶质的质量关系,故错误;
D、t2℃时的NaCl溶液与KNO3溶液中,溶质的质量分数不一定相等,若为饱和溶液,则该温度下其溶解度相等、溶质的质量分数也相等,现在溶液状态不确定,所以溶质的质量分数无法比较,故错误;
故选B.
点评:了解溶解度、溶质的质量分数、溶解度曲线的意义等知识,并会结合选项分析解答.

练习册系列答案
相关题目