题目内容
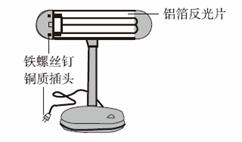
右图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验。
(1)小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的 等发生了化学反应。
(2)小红发现铝箔反光片呈银白色,无锈迹,原因是铝表面有一层致密的氧化膜,生成该氧化膜的化学方程式为 。
(3)铁、铝、铜的金属活动性由强到弱的顺序为 。为了验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,并利用台灯提供的一种金属进行实验,即达到了实验目的。实验中发生反应的化学方程式为 。
1)氧气和水蒸气(可填化学式) (2)4Al+3O2 2Al2O3
2Al2O3
(3)Al>Fe>Cu Fe+CuSO4 FeSO4+Cu
FeSO4+Cu
解析:(1)铁制品锈蚀的过程,是铁与空气中的氧气、水蒸气等发生化学反应的过程。(2)铝的化学性质比较活泼,它可与空气中的氧气反应生成一层致密的氧化铝薄膜,该变化中,反应物是铝(Al)和氧气(O2),生成物是氧化铝(Al2O3),据此可写出反应的化学方程式。(3)在金属活动性顺序中,三种金属由前到后的排列依次是Al、Fe、Cu,因此其金属活动性由强到弱的顺序为Al>Fe>Cu。因小志领取的药品是氯化铝溶液、硫酸铜溶液,台灯可提供铁,将铁分别放到两种溶液中,铁与氯化铝溶液不反应,说明铁的金属活动性比铝弱,铁可与硫酸铜溶液反应(铁表面覆盖一层红色的物质,溶液由蓝色变为浅绿色),说明铁的金属活动性比铜强,由此可达到实验目的,铁与硫酸铜溶液反应生成铜和硫酸亚铁,据此可写出反应的化学方程式。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

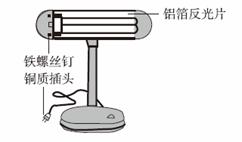
 进行观察分析并完成相关实验。
进行观察分析并完成相关实验。 活动性由
活动性由 强到弱的顺序为 。为了验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,并利用台灯提供的一种金属进行实验,即达到了实验目的。实验中发生反应的化学方程式为 。
强到弱的顺序为 。为了验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,并利用台灯提供的一种金属进行实验,即达到了实验目的。实验中发生反应的化学方程式为 。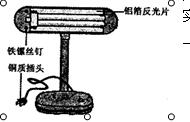
 进行观察分析并完成相关实验。
进行观察分析并完成相关实验。 活动性由
活动性由 强到弱的顺序为 。为了验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,并利用台灯提供的一种金属进行实验,即达到了实验目的。实验中发生反应的化学方程式为 。
强到弱的顺序为 。为了验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,并利用台灯提供的一种金属进行实验,即达到了实验目的。实验中发生反应的化学方程式为 。