题目内容
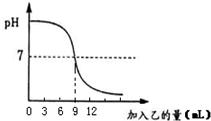 23、已知甲、乙分别是盐酸和氢氧化钠溶液中的一种.下图表示:向盛有10mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液时,溶液pH的变化曲线.请分析曲线回答问题:
23、已知甲、乙分别是盐酸和氢氧化钠溶液中的一种.下图表示:向盛有10mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液时,溶液pH的变化曲线.请分析曲线回答问题:(1)该反应的化学方程式为
NaOH+HCl=NaCl+H2O
(2)甲是
NaOH
溶液;滴有少量紫色石蕊试剂甲溶液呈
蓝
色.(3)当加入乙溶液的体积为
9
mL时,甲、乙溶液恰好完全反应.分析:氢氧化钠溶液和盐酸反应生成氯化钠和水,氢氧化钠溶液显碱性,其PH大于7,能使紫色石蕊试液变蓝,盐酸呈酸性,其PH小于7,与氢氧化钠恰好完全反应时溶液的PH等于7.
解答:解:(1)氢氧化钠溶液和盐酸反应生成氯化钠和水,所以本题答案为:NaOH+HCl=NaCl+H2O;
(2)从图象可以看出,开始时溶液的PH大于7,显碱性,表明甲是氢氧化钠溶液,能使石蕊试液变蓝,所以本题答案为:NaOH,蓝;
(3)盐酸与氢氧化钠恰好完全反应时溶液的PH等于7,从图象可以看出,此时加入盐酸的量为9mL,所以本题答案为:9.
(2)从图象可以看出,开始时溶液的PH大于7,显碱性,表明甲是氢氧化钠溶液,能使石蕊试液变蓝,所以本题答案为:NaOH,蓝;
(3)盐酸与氢氧化钠恰好完全反应时溶液的PH等于7,从图象可以看出,此时加入盐酸的量为9mL,所以本题答案为:9.
点评:此题考查了氢氧化钠与盐酸的反应,完成此题,可以依据已有的知识结合图象给出的信息进行.

练习册系列答案
相关题目
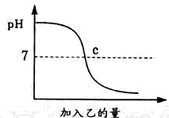 (2007?临沂)酸与碱作用生成盐和水的反应叫做中和反应.已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,下图表示向甲中加入乙时溶液pH的变化曲线.请写出你从曲线图中所获取的信息:
(2007?临沂)酸与碱作用生成盐和水的反应叫做中和反应.已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,下图表示向甲中加入乙时溶液pH的变化曲线.请写出你从曲线图中所获取的信息: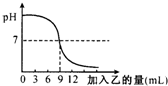 28、已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种.下图表示:向盛有10mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液时,溶液pH的变化曲线.请分析曲线回答问题:
28、已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种.下图表示:向盛有10mL稀的甲溶液(其中滴有少量紫色石蕊试剂)中,加入乙溶液时,溶液pH的变化曲线.请分析曲线回答问题: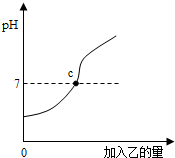 (2013?信阳一模)酸和碱能发生中和反应,生成盐和水.已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,图中表示向甲中加入乙时溶液pH的变化曲线,请你写出图中所获取的信息.(写三条)
(2013?信阳一模)酸和碱能发生中和反应,生成盐和水.已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,图中表示向甲中加入乙时溶液pH的变化曲线,请你写出图中所获取的信息.(写三条)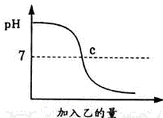 酸与碱作用生成盐和水的反应叫做中和反应.已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示向甲中加入乙时溶液pH的变化曲线.请写出你从曲线图中所获取的信息:
酸与碱作用生成盐和水的反应叫做中和反应.已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示向甲中加入乙时溶液pH的变化曲线.请写出你从曲线图中所获取的信息: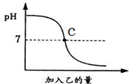 已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示向甲中加入乙时溶液pH的变化曲线.请写出你从曲线图中所获取的信息:
已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示向甲中加入乙时溶液pH的变化曲线.请写出你从曲线图中所获取的信息: