题目内容
(2004?金华)有一包固体粉末,可能由Na2C03、BaCl2、CuCl2、Na20中的一种或两种物质组成.将该粉末溶解于水,未出现浑浊现象.取所得溶液进行如下实验:
根据实验现象回答:
(1)写出滴加NaOH溶液反应的化学方程式______.
(2)写出试剂②的化学式______.
【答案】分析:将该粉末溶解于水,未出现浑浊现象.溶液中滴加氢氧化钠溶液产生蓝色沉淀,判断原固体粉末中一定有氯化铜,一定没碳酸钠;往无色溶液中滴加试剂①产生白色沉淀,试剂①的可能性较多,但再滴加足量的试剂②产生气泡,沉淀不消失,则推断白色沉淀是碳酸钡,试剂②就一定是硫酸.
解答:解:根据分析和实验现象得:
(1)溶液中滴加氢氧化钠溶液产生蓝色沉淀,判断原固体粉末中一定有氯化铜,滴加NaOH溶液反应的化学方程式:CuCl2+2NaOH═Cu(OH)2↓+2NaCl;
(2)往无色溶液中滴加试剂①产生白色沉淀,试剂①的可能性较多,但再滴加足量的试剂②产生气泡,沉淀不消失,则推断白色沉淀是碳酸钡,试剂②就一定是硫酸.试剂②的化学式:H2S04.
故答案为:(1)CuCl2+2NaOH═Cu(OH)2↓+2NaCl (2)H2S04.
点评:通过蓝色沉淀这明显物质为突破口,根据掌握酸碱盐的性质进行一一分析,推出各项结论.
解答:解:根据分析和实验现象得:
(1)溶液中滴加氢氧化钠溶液产生蓝色沉淀,判断原固体粉末中一定有氯化铜,滴加NaOH溶液反应的化学方程式:CuCl2+2NaOH═Cu(OH)2↓+2NaCl;
(2)往无色溶液中滴加试剂①产生白色沉淀,试剂①的可能性较多,但再滴加足量的试剂②产生气泡,沉淀不消失,则推断白色沉淀是碳酸钡,试剂②就一定是硫酸.试剂②的化学式:H2S04.
故答案为:(1)CuCl2+2NaOH═Cu(OH)2↓+2NaCl (2)H2S04.
点评:通过蓝色沉淀这明显物质为突破口,根据掌握酸碱盐的性质进行一一分析,推出各项结论.

练习册系列答案
相关题目
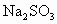 、
、 、
、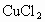 、
、 中的一种或两种物质组成.将该粉末溶解于水,未出现浑浊现象.取所得溶液进行如下实验:
中的一种或两种物质组成.将该粉末溶解于水,未出现浑浊现象.取所得溶液进行如下实验:
