题目内容
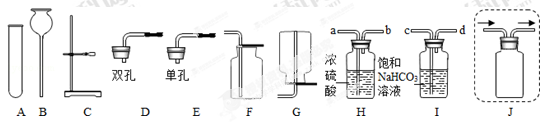
小组在实验室进行关于气体的实验,所用的部分仪器如下图所示。

(1)甲同学用双氧水制取氧气,发生反应的化学方程式是 ,选择的收集装置是D或 ,用 检验D收集满氧气。
(2)乙同学用氯酸钾和二氧化锰为原料制取氧气,二氧化锰的作用是 ,应选择的发生装置是 。该同学发现产生的气体能使带火星的木条复燃并有刺激性气味,下列分析不合理的是 。
a.反应中氧气的物理性质发生了变化
b.此时得到的气体一定是混合物
c.只加热氯酸钾,若生成的气体无气味,说明刺激性气味一定与二氧化锰有关
d.可能是生成的氧气与残留在发生装置中的空气在加热的条件下反应生成了新物质。
(3)丙同学研究了木条复燃与氧气体积分数的关系,发现不纯的氧气也能使带火星的木条复燃。右图F是他其中一次实验的装置,集气瓶中有约占总体积40%水,氧气从 导管口进入,排尽集气瓶中的水,收集氧气后集气瓶中氧气的体积分数是 。

(4)如图装置也可制取二氧化碳气体,制取二氧化碳的化学方程式为 。G装置的优点是可随时控制反应的发生和停止。若打开弹簧夹,固体与液体接触,反便能发生,请简述使G装置中反应停止的操作 。


(1)甲同学用双氧水制取氧气,发生反应的化学方程式是 ,选择的收集装置是D或 ,用 检验D收集满氧气。
(2)乙同学用氯酸钾和二氧化锰为原料制取氧气,二氧化锰的作用是 ,应选择的发生装置是 。该同学发现产生的气体能使带火星的木条复燃并有刺激性气味,下列分析不合理的是 。
a.反应中氧气的物理性质发生了变化
b.此时得到的气体一定是混合物
c.只加热氯酸钾,若生成的气体无气味,说明刺激性气味一定与二氧化锰有关
d.可能是生成的氧气与残留在发生装置中的空气在加热的条件下反应生成了新物质。
(3)丙同学研究了木条复燃与氧气体积分数的关系,发现不纯的氧气也能使带火星的木条复燃。右图F是他其中一次实验的装置,集气瓶中有约占总体积40%水,氧气从 导管口进入,排尽集气瓶中的水,收集氧气后集气瓶中氧气的体积分数是 。

(4)如图装置也可制取二氧化碳气体,制取二氧化碳的化学方程式为 。G装置的优点是可随时控制反应的发生和停止。若打开弹簧夹,固体与液体接触,反便能发生,请简述使G装置中反应停止的操作 。

(1)2H2O2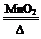 2H2O+O2↑ E 带火星的木条
2H2O+O2↑ E 带火星的木条
(2)催化剂 A ad
(3)b 52%
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑ 关闭弹簧夹
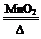 2H2O+O2↑ E 带火星的木条
2H2O+O2↑ E 带火星的木条(2)催化剂 A ad
(3)b 52%
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑ 关闭弹簧夹
试题分析:(1)甲同学用双氧水制取氧气,发生反应的化学方程式是2H2O2
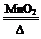 2H2O+O2↑,氧气可以用排水法和向下排空气法收集,氧气是用带火星的木条来检验的。(2)乙同学用氯酸钾和二氧化锰为原料制取氧气,二氧化锰的作用是催化剂,应选择的发生装置是固固加热型的装置,应选择A,a氧气的物理性质未发生改变,氧气不可能与空气中其他成分反应的,d错。(3)排水法收集氧气,氧气应从短导管进入,排尽装置内的水,说明进来40%的氧气,而原来60%的空气中,也存在氧气,氧气在空气中占20%,氧气占集气瓶的12%,加上进来的40%的氧气,所以瓶内氧气的体积分数为52%。(4)制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,关闭弹簧夹试管中压强变大,将液面向下压,液体会进入长颈漏斗中,当试管中的液面低于隔板的时候,两种药品不接触,反应即停止。
2H2O+O2↑,氧气可以用排水法和向下排空气法收集,氧气是用带火星的木条来检验的。(2)乙同学用氯酸钾和二氧化锰为原料制取氧气,二氧化锰的作用是催化剂,应选择的发生装置是固固加热型的装置,应选择A,a氧气的物理性质未发生改变,氧气不可能与空气中其他成分反应的,d错。(3)排水法收集氧气,氧气应从短导管进入,排尽装置内的水,说明进来40%的氧气,而原来60%的空气中,也存在氧气,氧气在空气中占20%,氧气占集气瓶的12%,加上进来的40%的氧气,所以瓶内氧气的体积分数为52%。(4)制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,关闭弹簧夹试管中压强变大,将液面向下压,液体会进入长颈漏斗中,当试管中的液面低于隔板的时候,两种药品不接触,反应即停止。
练习册系列答案
相关题目