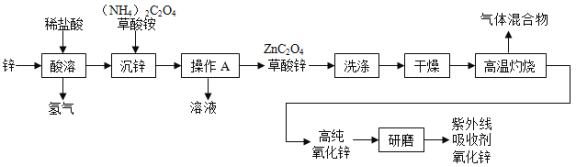
题目内容
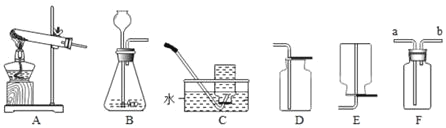
【题目】通过一学期的化学学习,你已经掌握了实验室制取气体的一些规律,以下是老师提供的一些实验装置,请你结合如图回答问题:
(1)写出实验室用氯酸钾和二氧化锰的混合物制备氧气的化学方程式_____,反应后二氧化锰的质量分数_____(填“增大”、“减少”或“不变”),实验完毕后发现试管已经炸裂,请分析炸裂原因:_____(答一种情况即可)。
(2)实验室用B装置可以制取的气体是_____,写出该反应的化学方程式_____。
(3)已知氨气是一种密度比空气小且极易溶于水的气体,其实验室制法的一种原理是氯化铵和氢氧化钠溶液在加热的情况下生成氯化钠、水、氨气,据此设计出的发生装置可以是_____,收集装置可以是_____(填“C”、“D”或“E”)。若用F装置进行密封收集氨气,气流应从_____端(“a”或“b”)流入集气瓶。
【答案】2KClO3![]() 2KCl+3O2↑ 增大 先熄灭酒精灯,后移出导管 氧气或二氧化碳 2H2O2
2KCl+3O2↑ 增大 先熄灭酒精灯,后移出导管 氧气或二氧化碳 2H2O2![]() 2H2O+O2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑或Zn+H2SO4=ZnSO4+H2↑ 固液加热型 E b
2H2O+O2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑或Zn+H2SO4=ZnSO4+H2↑ 固液加热型 E b
【解析】
(1)如果用氯酸钾制氧气需要加热,氯酸钾在二氧化锰作催化剂、加热的条件下生成氯化钾和氧气,反应过程中二氧化锰的质量不变,但反应后固体质量减少,所以反应后二氧化锰的质量分数增大;实验完毕后发现试管已经炸裂,炸裂原因是:先熄灭酒精灯,后移出导管,水倒流至试管导致试管炸裂。
(2)B装置是固液常温反应型装置,如果制氧气,则是用过氧化氢溶液制取氧气,过氧化氢在二氧化锰作催化剂的条件下生成水和氧气;如果用B装置制取CO2,是用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,还可以用锌粒和稀硫酸反应制氢气,反应生成硫酸锌和氢气,所以反应的化学方程式故填
2H2O2![]() 2H2O+O2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑或Zn+H2SO4=ZnSO4+H2↑;
2H2O+O2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑或Zn+H2SO4=ZnSO4+H2↑;
(3)验室制法的一种原理是氯化铵和氢氧化钠溶液在加热的情况下生成氯化钠、水、氨气,据此设计出的发生装置可以是:固液加热型;氨气是一种密度比空气小且极易溶于水的气体,因此只能用向下排空气法收集,故选E;若用F装置进行密封收集氨气,由于氨气的密度比空气的密度小,进入以后占据上方空间,空气被赶到下方空间而易从a端排出,故氨气应从b端进入。

 春雨教育同步作文系列答案
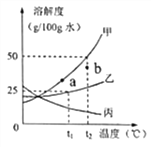
春雨教育同步作文系列答案【题目】根据下列溶解度曲线和A物质的部分温度是的溶解度判断下列说法正确的是( )
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | A物质 | 20 | 28 | 45 | 60 |
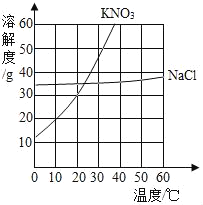
A. 由上图可知,KNO3和NaCl的溶解度均大于A 物质的溶解度
B. 10℃时,将40gNaCl放入50g水中,充分溶解,所得溶液是NaCl的不饱和溶液
C. 将30℃时NaCl、KNO3、和A物质的饱和溶液各降温至10℃,所得溶液的溶质质量分数大小为:KNO3>NaCl>A
D. 20℃时,将KNO3、NaCl和A物质各30g分别配制成恰好饱和溶液,所得溶液的质量大小为A>KNO3=NaCl