题目内容
下列叙述与图象反映的关系相符合的是( )
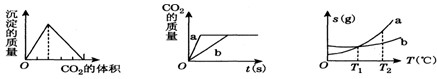
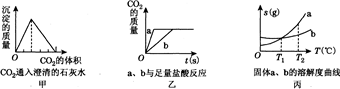
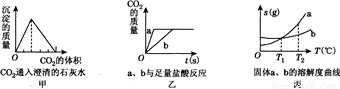
甲:CO2通入澄清的石灰水中 乙:a、b与足量盐酸反应 丙:固体a、b的溶解度曲线.

甲:CO2通入澄清的石灰水中 乙:a、b与足量盐酸反应 丙:固体a、b的溶解度曲线.
分析:A、二氧化碳可以和氢氧化钙反应生成沉淀,而当二氧化碳过量时碳酸钙沉淀会和二氧化碳反应生成可溶性的碳酸氢钙,可以据此分析该题;
B、本选项可以根据碳元素的质量守恒来作出判断;
C、根据溶解度曲线的意义及ab两物质的溶解度随温度变化情况来完成解答即可;
D、在比较不同物质的溶解度时必须指明所处的温度,可以据此作出判断.
B、本选项可以根据碳元素的质量守恒来作出判断;
C、根据溶解度曲线的意义及ab两物质的溶解度随温度变化情况来完成解答即可;
D、在比较不同物质的溶解度时必须指明所处的温度,可以据此作出判断.
解答:解:A、二氧化碳可以和氢氧化钙反应生成沉淀,而当二氧化碳过量时碳酸钙沉淀会和二氧化碳反应生成可溶性的碳酸氢钙,所以当通入二氧化碳之初就会产生沉淀,而当二氧化碳过量时沉淀的质量则会减少,直至全部溶解,由
Ca(OH)2+CO2=CaCO3↓+H2O…①
2CaCO3+2CO2+H2O═2Ca(HCO3)2…②
可以知道反应①中需要二氧化碳的质量和反应②消耗二氧化碳质量的相等,故体积也相等,而图中所给的二氧化碳的体积与分析不符,故A判断不正确;
B、碳酸氢钠的相对分子质量为84,而碳酸钠的相对分子质量为106,所以等质量的碳酸钠和碳酸氢钠含有的碳元素的质量不等,根据碳元素的质量守恒可以知道,等质量的碳酸氢钠和碳酸钠与足量的盐酸反应生成的二氧化碳的质量不可能相等,故B判断不正确;
C、根据溶解度曲线的意义可以知道,在温度为T1时ab的溶解度相等,所以此时两物质的饱和溶液的溶质的质量分数相等,当温度升高到T2时,它们的溶解度都要增大,所以溶液中溶质的质量分数不变,故C分析正确;
D、在比较不同物质的溶解度时必须指明所处的温度,而本题中没有指明温度,所以也就无从比较a和b的溶解度,故D判断不正确.
故选C.
Ca(OH)2+CO2=CaCO3↓+H2O…①
2CaCO3+2CO2+H2O═2Ca(HCO3)2…②
可以知道反应①中需要二氧化碳的质量和反应②消耗二氧化碳质量的相等,故体积也相等,而图中所给的二氧化碳的体积与分析不符,故A判断不正确;
B、碳酸氢钠的相对分子质量为84,而碳酸钠的相对分子质量为106,所以等质量的碳酸钠和碳酸氢钠含有的碳元素的质量不等,根据碳元素的质量守恒可以知道,等质量的碳酸氢钠和碳酸钠与足量的盐酸反应生成的二氧化碳的质量不可能相等,故B判断不正确;
C、根据溶解度曲线的意义可以知道,在温度为T1时ab的溶解度相等,所以此时两物质的饱和溶液的溶质的质量分数相等,当温度升高到T2时,它们的溶解度都要增大,所以溶液中溶质的质量分数不变,故C分析正确;
D、在比较不同物质的溶解度时必须指明所处的温度,而本题中没有指明温度,所以也就无从比较a和b的溶解度,故D判断不正确.
故选C.
点评:本题是过程与图象结合题,是对学生识图能力的考查,解题的关键是能正确的分析各个反应的过程,并结合图象分析问题,对培养学生分析问题的能力有一定帮助.

练习册系列答案
相关题目