题目内容
【题目】某化学兴趣小组在老师指导下制取、干燥、收集氨气,并探究氨气的一些性质.资料卡片:氨气通常情况下是有刺激性气味的无色气体,密度比空气小,极易溶于水,易液化,液氨可作制冷剂.加热熟石灰和氯化铵固体混合物的方法可以生成氨气,如要快速产生氨气,可以将浓氨水滴加到生石灰中得到.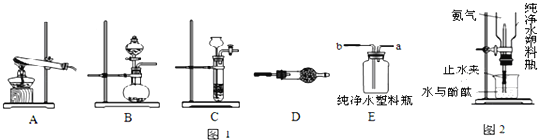
(1)利用A装置制取氨气的化学方程式为 .将浓氨水滴加到生石灰快速产生氨气,发生装置最好选用 (选填装置编号);请写出生石灰在此反应中的作用: (写一条即可).
(2)干燥氨气可以将气体通过装有 (填化学式)的装置D.
(3)兴趣小组计划用E装置收氨气,简述判断氨气已经集满的方法 .
(4)按图2连接仪器后,挤压纯净水塑料瓶会引发喷泉,为处理纯净水塑料瓶内存在的氨水(NH3H2O)可以加入少量稀硫酸,发生反应的化学方程式为 .
【答案】(1)Ca(OH)2+2NH4Cl![]() CaCl2+2H2O+2NH3↑;B;CaO遇水放热,降低了NH3的溶解度(合理均可);(2)CaO(或NaOH);(3)将湿润的红色石蕊试纸放在b端,若试纸变蓝色,说明氨气已经集满;(4)2NH3H2O+H2SO4=(NH4)2SO4+2H2O.
CaCl2+2H2O+2NH3↑;B;CaO遇水放热,降低了NH3的溶解度(合理均可);(2)CaO(或NaOH);(3)将湿润的红色石蕊试纸放在b端,若试纸变蓝色,说明氨气已经集满;(4)2NH3H2O+H2SO4=(NH4)2SO4+2H2O.
【解析】(1)利用A装置制取氨气的化学方程式为:Ca(OH)2 + 2NH4Cl ![]() CaCl2 + 2H2O + 2NH3↑;将浓氨水滴加到生石灰快速产生氨气,发生装置最好选用B装置;生石灰在此反应中的两个作用:CaO与水反应,减少了溶剂;CaO遇水放热,降低了NH3的溶解度.
CaCl2 + 2H2O + 2NH3↑;将浓氨水滴加到生石灰快速产生氨气,发生装置最好选用B装置;生石灰在此反应中的两个作用:CaO与水反应,减少了溶剂;CaO遇水放热,降低了NH3的溶解度.
(2)干燥氨气可以将气体通过装有CaO或NaOH的装置D;
(3)判断氨气已经集满的方法是:将湿润的红色石蕊试纸放在b端,若试纸变蓝色,说明氨气已经集满;
(4)氨水和浓硫酸反应的化学方程式为:2NH3H2O+H2SO4=(NH4)2SO4+2H2O;