题目内容
【题目】锂电池是-种新型的高能电池,质量轻、容量大,颇受手机、电脑等用户的青睐。某种锂电池的总反应式可表示为:![]() 。下列说法错误的是
。下列说法错误的是
A.LiMnO2属于氧化物
B.该反应前后锂元素的化合价发生了变化
C.该反应属于化合反应
D.MnO2中Mn的化合价为+4价
【答案】A
【解析】
A、氧化物是指含有两种元素,且一种是氧元素的化合物,LiMnO2是由三种元素组成的,故说法错误,符合题意;
B、反应前,锂单质中锂元素的化合价为零,反应后LiMnO2中锂元素的化合价为+1价,故说法正确,不符合题意;
C、该反应由两种物质生成了一种物质,属于化合反应,故说法正确,不符合题意;
D、二氧化锰中氧元素的化合价为-2价,根据各元素正负化合价的代数和为零原则计算可知锰元素显+4价,故说法正确,不符合题意;
故选:A。

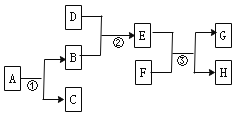
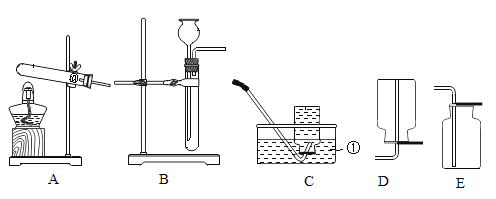
【题目】如下图是实验室制取气体的发生装置和气体收集装置。请你回答下列问题:
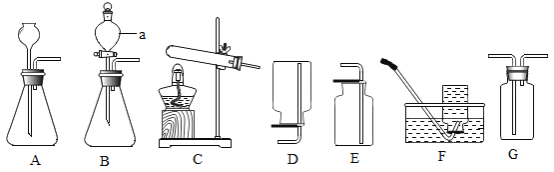
(1)仪器a的名称是________________________;
(2)实验室用过氧化氢溶液制取氧气,其反应的化学方程式是_______________________;若从控制反应速率和节约药品的角度考虑,应选择的发生装置是_______________________(填字母,下同)。
(3)实验室若用氯酸钾和二氧化锰(作催化剂)制取氧气,可选择装置_______________________作发生装置,其反应的化学方程式是________________________;
(4)D、E、F、G都是实验室中气体的收集装置,其中不能用来收集氧气的是________________________。
(5)某同学用上述(3)中的方法制取氧气,实验过程中试管发生了炸裂,请你帮他分析试管炸裂可能的原因是_______________________________________________。 (写一条即可)
(6)某校兴趣小组取氯酸钾和二氧化锰的混合物共3.0g放人大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
分析表中数据试计算原混合物中氯酸钾的质量分数是多少? ______________________(精确到0. 1%)
【题目】化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用20g石灰石样品,把80g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如右表:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入20g | 15g |
第二次加入20g | 10g |
第三次加入20g | 5g |
第四次加入20g | 3g |
(1)石灰石样品中碳酸钙的质量分数为______;
(2)第一次实验参加反应的碳酸钙的质量为______g;
(3)计算第一次加入20g稀盐酸充分反应后生成二氧化碳的质量__________。(写出计算过程)