题目内容
请你根据不同的实验内容,回答对应的问题:
| 实验名称 | 实验设计 | 分析和回答的问题 | ||||||||
| a.电解水 | 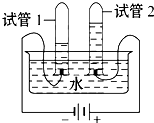 |
(1)试管1中产生的气体为 氢气 氢气 (填名称);该实验说明水是由氢元素和氧元素 氢元素和氧元素 组成的. | ||||||||
| b.空气中 | 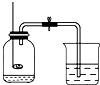 (燃烧匙中的药品为红磷) |
(2)实验中可观察到的现象是 红磷燃烧,集气瓶内充满白烟,打开弹簧夹后,水由烧杯流向集气瓶 红磷燃烧,集气瓶内充满白烟,打开弹簧夹后,水由烧杯流向集气瓶 ;某同学所得实验结果为集气瓶内的水上升至10%左右,其可能的原因是红磷量过少 红磷量过少 | ||||||||
| c.一氧化碳还原氧化铜 | 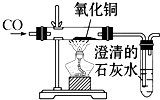 |
(3)写出该实验涉及的化学反应方程式: CO+CuO
CO+CuO .请你对如图所示的实验装置进行评价:
没有尾气处理装置. 没有尾气处理装置. |
分析:(1)根据电解水实验的现象和结论分析回答;
(2)根据测定空气中氧气含量的测定的实验的现象和注意的事项分析回答;
(3)CO具有还原性,能把CuO中的铜还原为单质铜,根据反应写出反应的方程式,根据一氧化碳有毒能污染空气分析评价装置的存在的问题.
(2)根据测定空气中氧气含量的测定的实验的现象和注意的事项分析回答;
(3)CO具有还原性,能把CuO中的铜还原为单质铜,根据反应写出反应的方程式,根据一氧化碳有毒能污染空气分析评价装置的存在的问题.
解答:解:(1)电解水时,电源的负极产生的气体是氢气,正极生成氧气,说明水是由氢元素和氧元素组成的.
(2)红磷燃烧时,集气瓶内充满白烟,打开弹簧夹后,水由烧杯流向集气瓶,流入集气瓶中水的体积应该是集气瓶空间体积的
左右.某同学所得实验结果为集气瓶内的水上升至10%左右,其可能的原因是:红磷量少、装置漏气或没有等到冷却至室温就打开弹簧夹等.
(3)CO具有还原性,能把CuO中的铜还原为单质铜,同时生成CO2.反应的方程式是:CO+CuO
Cu+CO2;由于反应中CO不可能全部反应,且CO也不与澄清的石灰水反应,故有毒的CO可能排放到空气中,所以应添加尾气处理装置.
故答为:(1)氢气 氢元素与氧元素;(2)红磷燃烧,集气瓶内充满白烟,打开弹簧夹后,水由烧杯流向集气瓶,红磷量过少;(3)CO+CuO
Cu+CO2,没有尾气处理装置.
(2)红磷燃烧时,集气瓶内充满白烟,打开弹簧夹后,水由烧杯流向集气瓶,流入集气瓶中水的体积应该是集气瓶空间体积的
| 1 |
| 5 |
(3)CO具有还原性,能把CuO中的铜还原为单质铜,同时生成CO2.反应的方程式是:CO+CuO
| ||
故答为:(1)氢气 氢元素与氧元素;(2)红磷燃烧,集气瓶内充满白烟,打开弹簧夹后,水由烧杯流向集气瓶,红磷量过少;(3)CO+CuO
| ||
点评:本题主要考查了课本中的几个重要探究实验,完成此题,可以依据已有的知识进行,要求同学们掌握常见的实验操作,以便灵活应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
请你根据不同的实验内容,回答对应的问题:
| 实验名称 | 实验设计 | 分析和回答的问题 |
| a.电解水 |  | (1)试管1中产生的气体为______(填名称);该实验说明水是由______组成的. |
| b.空气中 |  (燃烧匙中的药品为红磷) | (2)实验中可观察到的现象是______;某同学所得实验结果为集气瓶内的水上升至10%左右,其可能的原因是______ |
| c.一氧化碳还原氧化铜 |  | (3)写出该实验涉及的化学反应方程式:______.请你对如图所示的实验装置进行评价:______ |
 海水是一种化学成分复杂的混合物,包括水、溶解于水中的多种化学元素和气体.在海水中迄今已发现的化学元素达80多种.含量较高的元素除组成水的氢、氧元素外,还有氯、钠、镁、硫、钙、钾、溴、碳、锶、硼、氟等.
海水是一种化学成分复杂的混合物,包括水、溶解于水中的多种化学元素和气体.在海水中迄今已发现的化学元素达80多种.含量较高的元素除组成水的氢、氧元素外,还有氯、钠、镁、硫、钙、钾、溴、碳、锶、硼、氟等. A题:小明从某食品包装袋中取出一小包物质,部分标签如图:
A题:小明从某食品包装袋中取出一小包物质,部分标签如图: