题目内容
某气体既能用排水法收集,又能用向上排空气法收集,该气体的性质是
A.可溶于水,密度比空气小 B.难溶于水,密度比空气小
C.可溶于水,密度比空气大 D.难溶于水,密度比空气大
 名校课堂系列答案
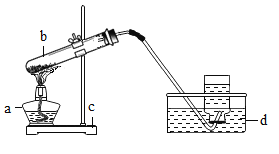
名校课堂系列答案自热火锅带有一个发热包(主要成分是生石灰),遇到水后在3~5秒钟内即可升温,温度可达150℃以上,蒸汽温度达200℃,最长保温时间可达3小时。自热火锅的发热过程无任何污染,成本低廉,但有一定的安全隐患。某校化学兴趣小组对一包久置的发热包成分进行了探究。
(猜想与假设)
猜想1:发热包成分为CaO和Ca(OH)2;
猜想2:发热包成分为Ca(OH)2和CaCO3;
猜想3:发热包成分为CaCO3;
猜想4:……
(进行实验)
实验操作 | 实验现象 | 实验结论 |
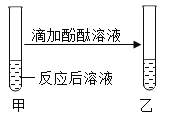
1.取少量样品于试管中,加适量水,振荡,手触摸试管外壁后,滴加几滴酚酞溶液 | ________ | 猜想2正确 |
2.另取少量样品于另一试管中,滴加足量的稀盐酸 | _____ |
操作2中发生的其中一个反应的化学方程式为____。
(继续探究)将实验后的废液倒入洁净的废液缸中,观察到溶液呈无色,该烧杯中的液体能否直接倒入下水道?同学们对其中的溶质成分继续进行了如下探究。
(猜想与假设)
猜想1:废液的溶质是CaCl2;
猜想2:废液的溶质是CaCl2、HCl;
猜想3:废液的溶质是CaCl2、Ca(OH)2。
你认为上述哪个猜想不合理?理由是____。为进一步确定该溶液的成分,小组成员继续设并完成了如下实验:
(设计实验)
实验操作 | 实验现象 | 实验结论 |
取少量废液于试管中,向其中加入 | ______ | 猜想2正确 |
(表达与交流)应向废液中加入适量____后再排放。
(反思与评价)如果废液不经过处理就排放,会造成的影响是____。
小明在做“盐酸中和氢氧化钠”的实验时,实验前忘记向氢氧化钠溶液中滴加酚酞溶液,导致无法判断中和反应进行的程度,于是小明对反应后溶液的酸碱性进行了探究。
(探究目的)确定反应后溶液的酸碱性
(猜想与假设)反应后溶液呈碱性,也可能呈_____,也可能呈_____。
(实验验证)
实验操作 | 实验现象 | 实验结论 |
| 无色酚酞溶液______ | 溶液呈碱性,使其呈碱性的微粒是_____ |
无色酚酞溶液不变色 | 溶液呈______ |
(继续验证)
实验操作 | 实验现象 | 实验结论 |
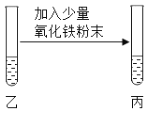
| 粉末部分或全部消失,溶液变为黄色 | 溶液呈_____,反应的化学方程式是_____ |
____________ | 溶液呈______ |