题目内容
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是
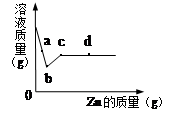
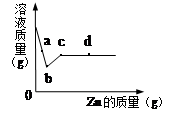
| A.a点溶液中的溶质有2种 |
| B.c点溶液中溶质为Zn(NO3)2 |
| C.若取b~c段溶液,滴加稀盐酸,有白色沉淀 |
| D.取d点的固体,加入稀盐酸,无气泡产生 |
B
试题分析:在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应
Zn+2AgNO3=Zn(NO3)2+2Ag
65 216
所以析出银的过程是溶液质量减少的过程;
Zn+Cu(NO3)2=Zn(NO3)2+Cu
65 64
所以析出铜的过程是溶液质量增加的过程
A、在a点时,硝酸银没有全部参加反应,溶液中含有硝酸银、硝酸铜和生成的硝酸锌,溶质是三种,故A错误; B、c点时硝酸铜恰好完全反应,溶液中只有硝酸锌,故B正确; C、b~c段是硝酸银全部参加反应完后锌和硝酸铜反应的过程,因此滴加稀盐酸,不会产生沉淀,故C错误; D、d点时锌过量,因此加入稀盐酸会产生氢气,故D错误;故选B.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目