题目内容
(2004?烟台)某中学环保小组在调查某化工厂的污水处理情况时,收集到如下资料:
①污水中的主要成分是盐酸,提取污水水样,测得其PH=3;
②处理污水的步骤之一是用石灰水与污水进行中和处理,使处理后反应池中的水样PH在7.0左右;
已知污水中HCl的质量分数为0.003%,若反应池中有2.0×106kg污水,至少需要多少千克氢氧化钙来处理这些污水?(污水中其他物质均不与石灰水反应;计算结果保留整数)
①污水中的主要成分是盐酸,提取污水水样,测得其PH=3;
②处理污水的步骤之一是用石灰水与污水进行中和处理,使处理后反应池中的水样PH在7.0左右;
已知污水中HCl的质量分数为0.003%,若反应池中有2.0×106kg污水,至少需要多少千克氢氧化钙来处理这些污水?(污水中其他物质均不与石灰水反应;计算结果保留整数)
分析:使处理后反应池中的水样pH在7.0左右,说明石灰水与盐酸恰好完全反应;根据反应的化学方程式,计算出处理污水需要氢氧化钙的质量.
解答:解:污水中氯化氢质量:2.0×106kg×0.003%=60kg
设至少需要氢氧化钙的质量为x
Ca(OH)2+2HCl=CaCl2+2H2O
74 73
x 60kg
=
解之得 x≈61kg
答:至少需要氢氧化钙的质量为61kg.
设至少需要氢氧化钙的质量为x
Ca(OH)2+2HCl=CaCl2+2H2O
74 73
x 60kg
| 74 |
| 73 |
| x |
| 60kg |
答:至少需要氢氧化钙的质量为61kg.
点评:根据化学方程式的基础计算,计算时注意溶液的质量不能带入化学方程式进行计算,要先计算中溶液中溶质质量.

练习册系列答案
相关题目
(2004
·烟台)享誉全国的“烟台苹果”已成为烟台农业经济的一个亮点.某果园苹果树因缺氮而枝叶生长不茂盛、叶色淡黄,可施加下列肥料中的[
]|
A . |
B . |
C . |
D .微量元素肥料 |
(2004
年烟台)享誉全国的“山东烟台苹果”已成为山东烟台农业经济的一个亮点.某果园苹果树枝生长不茂盛、叶色淡黄,可施加下列肥料中的[
]|
A . |
B .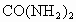 |
|
C .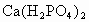 |
D .微量元素肥料 |
(2004
·烟台)享誉全国的“烟台苹果”已成为烟台农业经济的一个亮点.某果园苹果树因缺氮而枝叶生长不茂盛、叶色淡黄,可施加下列肥料中的[
]|
A .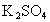 |
B . |
C .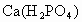 |
D .微量元素肥料 |