题目内容
【题目】某固体可能含有NaOH、NaCl、Na2CO3、CaCl2、MgCl2五种物质中的一种或几种,为确定其成分,相关实验及现象如下(微溶性物质按可溶性处理):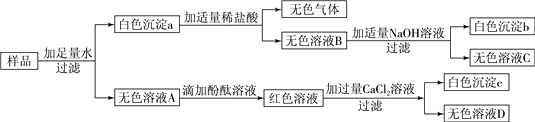
综合分析上述实验,回答下列问题。
(1)实验中生成的无色气体的化学式是;
(2)生成白色沉淀b反应的化学方程式是;
(3)无色溶液A中一定含有的溶质是;
(4)原固体中只有一种物质没有确定其是否存在,该物质是;
(5)A、B、C、D四种无色溶液中,能用来鉴别稀盐酸和Ca(OH)2溶液的是.
【答案】
(1)CO2
(2)MgCl2+2NaOH=Mg(OH)2↓+2NaCl
(3)NaCl、Na2CO3
(4)NaCl
(5)A、B、D
【解析】根据所学知识和题中信息知,(1)只有碳酸盐与盐酸反应生成气体。实验中生成的无色气体的化学式是CO2;(2)生成白色沉淀b反应的化学方程式是MgCl2+2NaOH=Mg(OH)2↓+2NaCl ;(3)无色溶液A中一定含有的溶质是Na2CO3,和NaCl;(4)原固体中只有一种物质没有确定其是否存在,该物质是NaCl ;(5)A、B、C、D四种无色溶液中,能用来鉴别稀盐酸和Ca(OH)2溶液的是A、B、D;
所以答案是:(1)CO2;(2)MgCl2+2NaOH═Mg(OH)2↓+2NaCl;(3)NaCl、Na2CO3;(4)NaCl;(5)A、B、D
【考点精析】掌握书写化学方程式、文字表达式、电离方程式是解答本题的根本,需要知道注意:a、配平 b、条件 c、箭号.

练习册系列答案
相关题目