题目内容
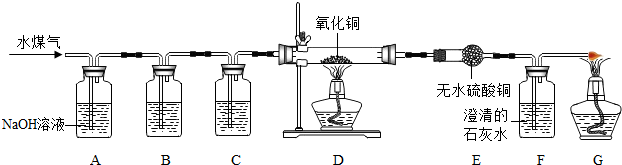
水煤气的主要成分是CO和H2(少量CO2和水蒸气),某同学通过下列实验,验证水煤气的主要成分,请根据如图所示装置,回答有关问题.
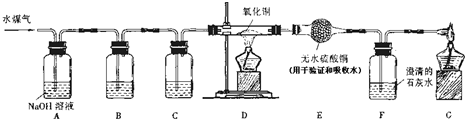
(1)A装置中反应的化学方程式是
(2)为了是检验水煤气中的CO2是否已除尽,应在B装置内盛放的物质是
(3)C装置内盛放的物质是浓硫酸,其作用是
(4)D装置内的现象是
(5)从环保角度来说,装置G的重要作用是

(1)A装置中反应的化学方程式是
CO2+2NaOH═Na2CO3+H2O
CO2+2NaOH═Na2CO3+H2O
;(2)为了是检验水煤气中的CO2是否已除尽,应在B装置内盛放的物质是
澄清的石灰水
澄清的石灰水
;(3)C装置内盛放的物质是浓硫酸,其作用是
吸水干燥
吸水干燥
;(4)D装置内的现象是
黑色粉末变成红色
黑色粉末变成红色
;(5)从环保角度来说,装置G的重要作用是
因为一氧化碳有毒,防止一氧化碳污染空气
因为一氧化碳有毒,防止一氧化碳污染空气
;写出此处进行的一个化学反应方程式2CO+O2
2CO2
| ||
2CO+O2
2CO2
.
| ||
分析:(1)根据A中氢氧化钠溶液只可与水煤气中的二氧化碳反应,写出化学反应式;
(2)B装置内的物质澄清的石灰水可以检验二氧化碳是否被除尽;
(3)C装置中的浓硫酸具有吸水性;
(4)一氧化碳在加热的条件下还原氧化铜,使黑色粉末变成红色;
(5)根据一氧化碳的毒性分析.
(2)B装置内的物质澄清的石灰水可以检验二氧化碳是否被除尽;
(3)C装置中的浓硫酸具有吸水性;
(4)一氧化碳在加热的条件下还原氧化铜,使黑色粉末变成红色;
(5)根据一氧化碳的毒性分析.
解答:解:(1)A中氢氧化钠溶液只可与水煤气中的二氧化碳反应,生成碳酸钠和水,反应的方程式为:CO2+2NaOH═Na2CO3+H2O;
(2)B装置的作用是检验二氧化碳是否被除尽,所以应盛放澄清的石灰水;
(3)因为浓硫酸具有吸水性,可以把把剩余的水分除去,所以C装置中浓硫酸的作用是吸水干燥;
(4)剩余的CO和H2可以还原D装置中的黑色氧化铜,生成红色的铜,所以D装置的现象是黑色粉末变成红色;
(5)因为一氧化碳有毒,属于要进行尾气处理;反应的方程式为:2CO+O2
2CO2
故答案为:
(1)CO2+2NaOH═Na2CO3+H2O;
(2)澄清的石灰水;
(3)吸水干燥;
(4)黑色粉末变成红色;
(5)因为一氧化碳有毒,防止一氧化碳污染空气;2CO+O2
2CO2
(2)B装置的作用是检验二氧化碳是否被除尽,所以应盛放澄清的石灰水;
(3)因为浓硫酸具有吸水性,可以把把剩余的水分除去,所以C装置中浓硫酸的作用是吸水干燥;
(4)剩余的CO和H2可以还原D装置中的黑色氧化铜,生成红色的铜,所以D装置的现象是黑色粉末变成红色;
(5)因为一氧化碳有毒,属于要进行尾气处理;反应的方程式为:2CO+O2
| ||
故答案为:
(1)CO2+2NaOH═Na2CO3+H2O;
(2)澄清的石灰水;
(3)吸水干燥;
(4)黑色粉末变成红色;
(5)因为一氧化碳有毒,防止一氧化碳污染空气;2CO+O2
| ||
点评:本题考查知识点较多,有化学反应式的书写、二氧化碳与石灰水的反应、浓硫酸的作用、一氧化碳还原氧化铜的实验的现象等,需同学们对化学知识有全面的了解.

练习册系列答案
相关题目
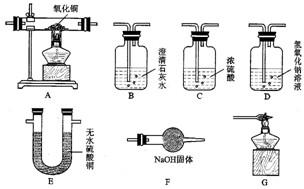 17、如图是实验室提供的实验装置,以供下列各种实验选择.工业上使用的未经净化的水煤气中含有CO、H2、CO2和水蒸气.请你利用以上实验装置装配一套证明水煤气的主要成分是CO和H2的实验装置.
17、如图是实验室提供的实验装置,以供下列各种实验选择.工业上使用的未经净化的水煤气中含有CO、H2、CO2和水蒸气.请你利用以上实验装置装配一套证明水煤气的主要成分是CO和H2的实验装置.