题目内容
有40g质量分数10%的NaCl溶液,若将其质量分数为20%,可采用( )A.加入5gNaCl固体
B.把溶剂蒸发掉5g
C.把溶剂蒸发20g
D.加入40g10%的NaCl溶液
【答案】分析:要想将10%的NaCl溶液变为20%,其实就是稀溶液变浓,其方法就是①加入一定量的溶质氯化钠②蒸发一定量的溶剂③加入更浓的溶液.具体加溶质多少或者蒸发多少溶剂或者加多少浓溶液根据溶质的质量分数公式进行计算即可.
解答:解:原溶液中溶质的质量=40×10%=4(克),溶剂的质量=40-4=36(克)
A、设加入溶质氯化钠X克,根据溶质的质量分数= ×100%=
×100%= ×100%=20%,解得X=5(克);故正确
×100%=20%,解得X=5(克);故正确
B、设蒸发溶剂的质量为X克,溶质不变由溶质的质量分数= ×100%=
×100%=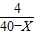 ×100%=20%,解得X=20(克);故错误
×100%=20%,解得X=20(克);故错误
C、由B计算可知其说法是对的;故正确
D、因为所加的溶液的浓度与原先的溶液浓度相同10%,根据溶液的特征可知那么所得溶液的浓度不变;故错误
故选:A、C
点评:本题考查了稀溶液变浓的方法,通常有三种方法:①加溶质②蒸发溶剂③加入比所配制溶液浓度更大的溶液;对于具体情况下加入多少,根据溶质的质量分数可以计算所得.
解答:解:原溶液中溶质的质量=40×10%=4(克),溶剂的质量=40-4=36(克)
A、设加入溶质氯化钠X克,根据溶质的质量分数=
 ×100%=
×100%= ×100%=20%,解得X=5(克);故正确
×100%=20%,解得X=5(克);故正确B、设蒸发溶剂的质量为X克,溶质不变由溶质的质量分数=
 ×100%=
×100%=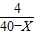 ×100%=20%,解得X=20(克);故错误
×100%=20%,解得X=20(克);故错误C、由B计算可知其说法是对的;故正确
D、因为所加的溶液的浓度与原先的溶液浓度相同10%,根据溶液的特征可知那么所得溶液的浓度不变;故错误
故选:A、C
点评:本题考查了稀溶液变浓的方法,通常有三种方法:①加溶质②蒸发溶剂③加入比所配制溶液浓度更大的溶液;对于具体情况下加入多少,根据溶质的质量分数可以计算所得.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
有40g质量分数10%的NaCl溶液,若将其质量分数为20%,可采用( )
| A、加入5gNaCl固体 | B、把溶剂蒸发掉5g | C、把溶剂蒸发20g | D、加入40g10%的NaCl溶液 |