题目内容
【题目】某校同学在老师的指导下,设计了如下实验装置进行气体制取和性质的探究:
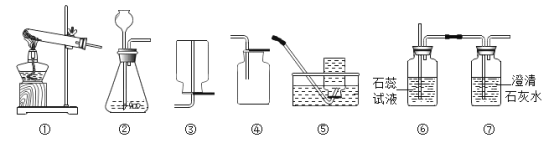
(1)利用图中所示装置,采用以下组合能完成实验室制取气体的有___________(填字母)。
A用①③制取氧气
B用②⑤制取氧气
C用②④制取氢气
D用②⑤制取二氧化碳
(2)若装置B中反应剧烈,从实验安全角度考虑,可以将长颈漏斗换成____________来控制液体的滴加速度;
(3)某同学用图中①⑥⑦装置组合制取二氧化碳气体并验证相关性质。则装置⑥中反应现象是___________。
【答案】B 分液漏斗 紫色溶液变红色
【解析】
(1)制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热。氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集。实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热。二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集。实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;
(2)分液漏斗可以控制反应的速率;
(3)二氧化碳和水反应生成碳酸,石蕊遇碳酸变红。
(1)A、氧气的密度比空气的密度大,氧气不能用向下排空气法收集,故A错误;
B、如果用双氧水和二氧化锰制氧气就不需要加热,氧气不易溶于水,因此能用排水法收集,故B正确;
C、氢气密度比空气的密度小,氢气不能用向上排空气法收集,故C错误;
D、二氧化碳能溶于水,不能用排水法收集,故D错误;
故答案为:B;
(2)分液漏斗可以控制液体药品的滴加速度来控制反应的速率,故答案为:分液漏斗;
(3)⑥装置中反应现象是:紫色变红色,因为二氧化碳和水反应生成碳酸,石蕊遇碳酸变红;故答案为:紫色变红色。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】下表为氯化铵和氯化钠在不同温度时的溶解度,回答下列问题:
温度/°C | 0 | 10 | 20 | 30 | 40 | 50 |
NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)由表中数据可知,溶解度随温度变化较大的物质是____________。
(2)20°C时75g水中最多只能溶解NaCl__________g;氯化钠与氯化铵溶解度相等的温度在_________°C之间。
(3)向烧杯中加入100g水和50. 0g氯化铵配制成50°C的溶液,再冷却到30°C ,烧杯中析出固体的质量为___________g。
【题目】如表是几种家用清洁剂的功能和有效成分.
清洁剂 |
洁厕灵 |
彩漂液 |
漂白水 |
功 能 | 清除污垢,除异味 | 漂洗衣物,使色彩鲜艳 | 漂除衣物污渍 |
有效成分 | 盐酸(HCl) | 过氧化氢 | 次氯酸钠(NaClO) |
根据表中信息,回答下列问题.
(1)HCl中氯元素的化合价为 .
(2)若大理石的污垢用洁厕灵清洗,主要现象是 .
(3)在盛有少量“彩漂液”的试管中,加少量二氧化锰,发生反应的化学方程式为 .
(4)“洁厕灵”与“漂白水”不能混用.二者若混合,其有效成分之间能发生化学反应,产生氯化钠、水和有毒的氯气(Cl2),化学方程式为 .