题目内容
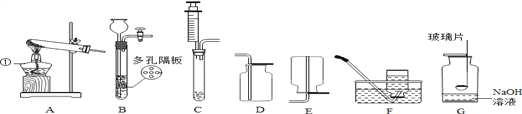
【题目】下图是实验室常用装置,回答下列问题:
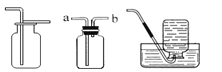
A B C D E
(1)实验室用氯酸钾制取氧气,应选用气体发生装置____ ,若用装置D收集氧气,验满方法是_____________。若用过氧化氢制氧气,应选用的制取装置是 _____,反应的化学方程式是____________________,若用高锰酸钾制氧气,A中还缺少的用品是______,该反应的化学方程式是___________________。用装置D采用排水法收集氧气,气体应从______(a或b)通入。电解水也能得到氧气,请写出反应的化学方程式___________________。
(2)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;②氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。小芳同学加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的反应的气体发生装置是____,请写出氨气和氧化铜在加热的条件下反应的化学反应方程式____________________________________。
【答案】 A 带火星木条放在b处复燃则满 BC/BD/BE 2H2O2![]() 2H2O+O2↑ 棉花 2KMnO4
2H2O+O2↑ 棉花 2KMnO4![]() K2MnO4+MnO2+O2↑ b 2H2O
K2MnO4+MnO2+O2↑ b 2H2O![]() 2H2↑ +O2↑ A 2NH3+3CuO
2H2↑ +O2↑ A 2NH3+3CuO![]() 3Cu+3H2O+N2
3Cu+3H2O+N2
【解析】氯酸钾制取氧气的条件是加热,故选固固加热型装置A;D是排空气法收集氧气的装置,验满时将带火星的木条置于瓶口,如复燃则满;过氧化氢制取氧气 的条件是不加热,选择固液不加热型装置B,收集时可选CDE;化学反应方程式为2H2O2![]() 2H2O+O2↑ ;高锰酸钾制取氧气时管口要放棉花,防止高锰酸钾堵塞导管; 该反应方程式为2KMnO4
2H2O+O2↑ ;高锰酸钾制取氧气时管口要放棉花,防止高锰酸钾堵塞导管; 该反应方程式为2KMnO4![]() K2MnO4+MnO2+O2↑;装置D为多功能装置,因氧气的密度比水的密度小,故是b进出;电解水制取氧气的化学反应方程式为2H2O
K2MnO4+MnO2+O2↑;装置D为多功能装置,因氧气的密度比水的密度小,故是b进出;电解水制取氧气的化学反应方程式为2H2O![]() 2H2↑ +O2↑;
2H2↑ +O2↑;
(2)有题可知,制取氨气的条件是加热,故选固固加热型装置A,氨气与氧化铜反应 方程式为2NH3+3CuO![]() 3Cu+3H2O+N2。
3Cu+3H2O+N2。

【题目】合金的种类很多,用途非常广泛,黄铜是铜和锌的合金,它可以用来制造机器和电器的零件等,化学兴趣小组的同学欲测定实验室中某铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。
称量10g粉末状黄铜样品放入烧杯中,量取45mL稀盐酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | |
加入稀盐酸的体积(ml) | 15 | 15 | 15 |
生成氢气的质量(g) | 0.04 | m | 0.02 |
试求:
(1)m的数值 。
(2)此黄铜样品中铜的质量分数是多少?(写出计算过程)