题目内容
【题目】水是一种重要的资源。请回答下列问题:
(1)下列说法正确的是_________(填序号)。
A.软水加入肥皂水容易起浮渣 B.生活中常用煮沸的方法降低水的硬度
C.活性炭在净水中起到吸附作用 D.自来水厂经过沉淀、过滤、吸附、消毒等可将泉水变成纯净水
(2)如图所示为X、Y、Z三种固体物质的溶解度曲线,请回答下列问题:
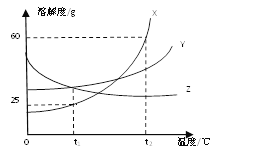
①t1℃时,三种物质溶解度的大小关系是___________。
②要将t2℃时X的饱和溶液变成不饱和溶液,可采取的措施有:升高温度、___________等。
③将t2℃时溶质质量分数为25%的X溶液降温到t1℃,所得溶液中溶质质量分数是___________。
【答案】 B C Y=Z>X 加溶剂 20%
【解析】(1)A、肥皂水可以检验软硬水,浮渣少,泡沫多的是软水,故错误;
B、煮沸可以将水中可溶性的钙镁化合物转化为难溶性的钙镁化合物沉淀出来,故可以降低水的硬度,故正确;
C、活性炭具有吸附性,可以吸附色素和异味,故在净水中起到吸附作用,故正确;
D、自来水厂经过沉淀、过滤、吸附、消毒等过程只能除去水中的难溶性杂质,水中的可溶性杂质不能除去,故不能将泉水变成纯净水,故错误。故选BC;
(2)由溶解度曲线可知,X物质的溶解度随温度的升高而升高,故将将t2℃时X的饱和溶液变成不饱和溶液,可采取的措施有升高温度或加入溶剂;
t1℃X的溶解度是25g,故该温度下溶质质量分数为![]() ×100%=20%,说明t2℃时溶质质量分数为25%的X溶液降温到t1℃时,变为饱和溶液,故溶质的质量分数为20%。
×100%=20%,说明t2℃时溶质质量分数为25%的X溶液降温到t1℃时,变为饱和溶液,故溶质的质量分数为20%。

【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
A | B |
太阳能吸附式制冷结露法空气取水器可在野外获取淡水,吸附剂中主要物质为SiO2和CaCl2。 (1)SiO2属于________(填字母序号)。 A.氧化物 B.化合物 C.混合物 (2)CaCl2中钙元素的质量分数为________(写出计算式即可)。 | 水净化过程中常用的消毒剂有:O3、Cl2、Ca(ClO)2、ClO2。 (1)上述物质中,只含一种元素的物质是________。 (2)Ca(ClO)2中钙元素与氧元素的质量比为________。 |