题目内容
【题目】某工厂欲从只含有 CuSO4 的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
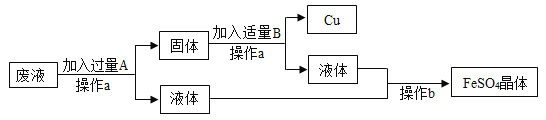
请回答下列问题:
(1)操作 a 的名称是 。
(2)写出流程中有关反应的化学方程式: 、 。以上两个反应能够发生的原因是
【答案】(1)过滤(2)Fe+CuSO4=FeSO4+Cu;Fe+H2SO4=FeSO4+H2↑;在金属活动性顺序中,铁位于铜、氢之前
【解析】
试题分析:(1)经过过滤操作a能将难溶固体和液体分离,(2)经过操作a得到的液体中能得到硫酸亚铁,说明回收铜时加入的是铁,多余的铁与稀硫酸反应生成硫酸亚铁;有关反应的化学方程式为:Fe+CuSO4=FeSO4+Cu; Fe+H2SO4=FeSO4+H2↑金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au。在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。以上两个反应能够发生的原因是在金属活动顺序中,铁的活动性位于铜,氢的之前.在金属活动顺序中,铁的活动性位于铜

练习册系列答案
相关题目