题目内容
除去下列物质中所含杂质,选用的试剂(括号内的物质)正确的是
| A.CaO中混有少量CaCO3(盐酸) |
| B.Cu(NO3)2溶液中混有AgNO3(铜粉) |
| C.CO2中混有HCl气体(NaOH溶液) |
| D.CO2中混有少量CO(氧气) |
B
试题分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质:A.氧化钙和碳酸钙均能与盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故A错误;B.铜与硝酸银反应生成硝酸铜和银,过滤后将银除去,最后就只剩硝酸铜了,故B正确;C.CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则;故C错误;D.除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为,当二氧化碳大量存在时,少量的一氧化碳不能与氧气充分接触,不会燃烧,故D错误,故选B

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目



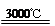 Si(粗)+2CO
Si(粗)+2CO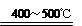 SiCl4
SiCl4  Si(纯)+4HCl
Si(纯)+4HCl