题目内容
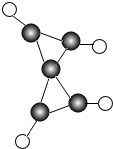
科学家最近在-100℃的低温下合成了一种化合物X,如图为此分子的模型,其中每个 代表一个碳原子,每个
代表一个碳原子,每个 代表一个氢原子.下列说法中不正确的是( )
代表一个氢原子.下列说法中不正确的是( )
 代表一个碳原子,每个
代表一个碳原子,每个 代表一个氢原子.下列说法中不正确的是( )
代表一个氢原子.下列说法中不正确的是( )| A.该分子的分子式为C4H5 |
| B.该分子中碳元素的质量分数是93.75% |
| C.该分子中的氢原子与碳原子的个数比是4:5 |
| D.等质量的该物质与甲烷相比,燃烧时消耗的氧气更多 |

A、由该物质的分子模型图可知该物质的分子由五个碳原子和四个氢原子所构成,因此该物质的化学式可写为C5H4;故A不正确;
B、该分子中碳元素的质量分数=
×100%=93.75%;故B正确;
C、由该物质的化学式C5H4可知该分子由5个C原子和4个H原子构成,因此该分子中的氢原子与碳原子的个数比是4:5;故C正确;
D、要解答这个问题,可根据方程式中两种物质与氧气的质量比求解,化学方程式如下:
CH4+2O2
CO2+2H2O
1664
C5H4 +6O2
5CO2+2H2O
64 192
甲烷燃烧的化学反应中甲烷与氧气的质量比是16:64=1:4,C5H4燃烧的反应中C5H4与氧气的质量比是64:192=1:3,相当于每1克的两种物质燃烧,甲烷消耗氧气的质量是4克、该化合物消耗氧气的质量是3克,显然等质量的该物质与甲烷相比,燃烧时消耗的氧气少. 故D不正确;
故选AD
B、该分子中碳元素的质量分数=
| 12×5 |
| 12×5+1×4 |
C、由该物质的化学式C5H4可知该分子由5个C原子和4个H原子构成,因此该分子中的氢原子与碳原子的个数比是4:5;故C正确;
D、要解答这个问题,可根据方程式中两种物质与氧气的质量比求解,化学方程式如下:
CH4+2O2
| ||
1664
C5H4 +6O2
| ||
64 192
甲烷燃烧的化学反应中甲烷与氧气的质量比是16:64=1:4,C5H4燃烧的反应中C5H4与氧气的质量比是64:192=1:3,相当于每1克的两种物质燃烧,甲烷消耗氧气的质量是4克、该化合物消耗氧气的质量是3克,显然等质量的该物质与甲烷相比,燃烧时消耗的氧气少. 故D不正确;
故选AD

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 的粒子,当X=10,其粒子的名称叫______;当X=8时,其粒子的符号为______.当X=11,其粒子的符号为______.其中离子间由于______作用而形成化合物的化学式为______,名称叫______.
的粒子,当X=10,其粒子的名称叫______;当X=8时,其粒子的符号为______.当X=11,其粒子的符号为______.其中离子间由于______作用而形成化合物的化学式为______,名称叫______.
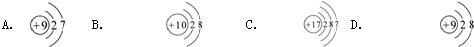
 ”代表氢原子,“
”代表氢原子,“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子).下列叙述中,不正确的是( )
”代表氧原子).下列叙述中,不正确的是( )

 ”表示氢原子、“
”表示氢原子、“ ”表示氧原子,表示一个水分子的是( )
”表示氧原子,表示一个水分子的是( )


